Clínica de Alergia e Pneumologia
Avenida do Contorno 4852 Sl 201
Belo Horizonte - MG
Telefone: (31) 3221-9900
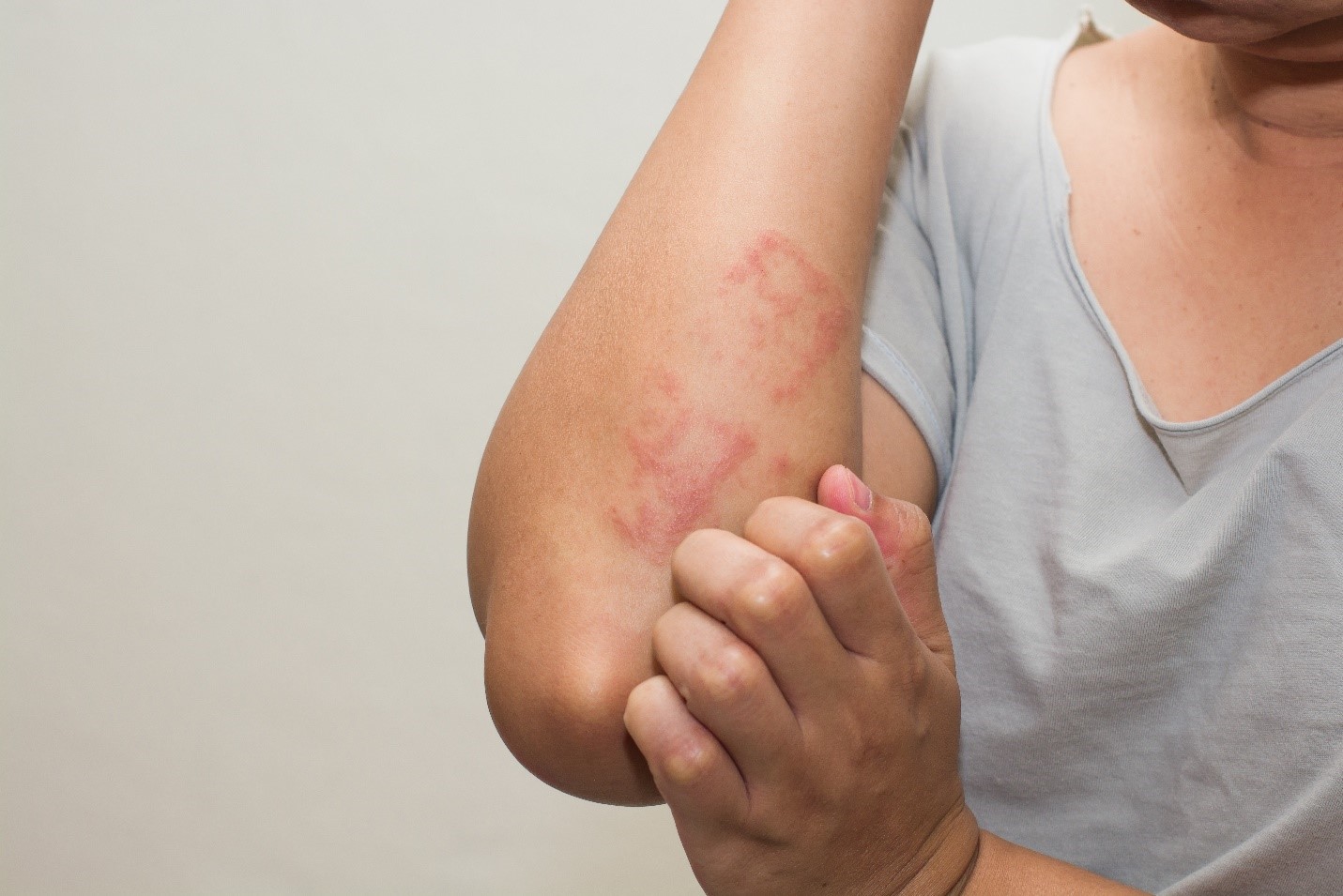
Asma - Rinites - Urticárias - Dermatites - Bronquites - Tosse Crônica - Pruridos


A IMPORTÂNCIA DO CONTROLE AMBIENTAL
A previsão é alarmante: até o fim deste século, metade da população humana deverá sofrer de algum tipo de alergia. Segundo a Organização Mundial de Saúde (OMS), a doença ataca atualmente 30% dos habitantes do planeta, o equivalente a 2 bilhões de pessoas. No Brasil, a legião de alérgicos é proporcionalmente ainda maior. Dados da Sociedade Brasileira de Alergia e Imunopatologia (SBAI) mostram que 35% dos brasileiros padecem do mal. A maioria sofre de asma, doença alérgica que mata cerca de 2 mil pessoas por ano no país e foi a quinta maior causa de internação no Sistema Único de Saúde (SUS) em 2002, segundo o Ministério da Saúde. 'A vida em ambientes fechados, o menor contato com a natureza e os animais, a produção de novos materiais e a elevação da poluição ambiental são alguns dos fatores que fazem com que um número cada vez maior de pessoas adquira alergias', afirma o alergista Ataualpa Reis, diretor da ASBAI
As alergias resultam de uma combinação da bagagem genética individual, que torna o organismo de algumas pessoas mais sensível, com fatores agressivos presentes no ambiente, chamados alérgenos. Os mais comuns estão dentro do próprio domicílio. São os ácaros encontrados na poeira, restos e fezes de baratas, mofo, pêlos de animais domésticos, fumaça de cigarro, pólen e esporos de fungos, além de certos alimentos, medicamentos e produtos químicos.
Quando uma pessoa alérgica entra em contato com algum desses agentes, seu sistema de defesa reage de forma exagerada, produzindo os sintomas desconfortáveis das alergias. Vide o filme sobre estas reações em anexo.
Os sintomas mais freqüentes das alergias respiratórias incluem espirros constantes, coriza, sensação de nariz entupido ou de “cabeça pesada”, coceira nos olhos, no nariz, no céu da boca e na garganta. Já nas crises de asma, os pacientes têm “chiado”, tosse, falta de ar, sensação de “aperto” no peito e cansaço. O incômodo é maior sobretudo à noite ou ao acordar e tende a piorar com esforço físico.
A asma brônquica é uma das doenças alérgicas mais preocupantes já que atinge uma de cada quatro crianças na faixa dos 6 aos 14 anos, conforme um estudo internacional (ISAAC) concluído em 1998 e confirmado em 2003 e 2006 com publicação internacional no Lancet. Os casos mais graves geram 370 mil internações por ano no País e gastos da ordem de R$ 76 milhões de dólares para o Sistema Único de Saúde(Datasus-2003). Sem contar que a mortalidade por asma dobrou nos últimos 30 anos e alcança hoje 6 mortes notificadas por dia(Datasus-2003-Gov. do Brasil).
Uma das principais formas de deter as crises é fazer o tratamento preventivo medicamentoso, sob a orientação médica. Outro cuidado fundamental é manter os ambientes limpos, livres de ácaros e poeira: encape colchões e travesseiros com tecidos impermeáveis; use pano úmido e produtos que eliminem o mofo no chão e nas paredes; remova tapetes, cortinas e bichinhos de pelúcia; deixe os ambientes ventilados e iluminados pelo sol. E – muito importante – não permita cigarro em locais fechados e perto de crianças.
Para prevenir as alergias respiratórias e a asma
· Manter os ambientes secos e abertos, permitindo a circulação do ar e a entrada dos raios de sol, capazes de destruir os ácaros
· Incentivar as crianças a brincar ao ar livre, agasalhando-as no tempo de frio
· Encapar colchões, travesseiros e almofadas com plástico ou tecidos impermeáveis
· Trocar a roupa de cama pelo menos uma vez por semana, lavando-a em água quente
· Usar cobertores antialérgicos, lavando-os regularmente e deixando ao sol para secar
· Evitar plantas, animais de estimação, bichinhos de pelúcia, tapetes ou carpetes, livros e brinquedos acumulados no quarto das crianças
· Retirar as cortinas ou usar aquelas de tecido sintético, mais finas, curtas e presas por argolas para facilitar a remoção e a lavagem a cada 15 dias
· Substituir a vassoura por pano úmido na limpeza diária, afastando as pessoas alérgicas
· Aplicar produtos antimofo nos locais úmidos e sujeitos a mofos
· Não usar inseticidas em spray nem espiral
· Jamais fumar dentro de casa, perto de crianças ou mesmo de adultos alérgicos
ATAUALPA P. DOS REIS-MÉDICO ALERGOLOGISTA TITULADO PELA ASSOCIAÇÃO BRASILEIRA DE ALERGIA E IMUNOPATOLOGIA E PROFESSOR DE POS GRADUAÇÃO CONVIDADO DA UFMG E SANTA CASA DE BELO HORIZONTE-www.clinnicaalergiaepneumologia.com.br -Clínica de Alergia e Pneumologia Dr. Ataualpa P.Reis
A intervenção precoce nas doenças alérgicas em pediatria
Early intervention in allergic diseases in pediatrics.How and When
La intervención precoz en las doenças alérgicas en pediatria. Cómo e cuándo
Artigo Especial
A intervenção precoce nas doenças alérgicas
Ataualpa P. Reis
Pós Doc da Duke University-USA e National Medical Research Center-
London
Professor de Pós Graduação Convidado do Instituto de Ciências
Biológicas da UFMG e da Santa Casa de Misericórdia de Belo Horizonte
A intervenção precoce nas doenças alérgicas em pediatria.Como e quando intervir
Resumo
Objetivo: Estudos epidemiológicos e da história natural das doenças alérgicas têm encontrado que na maioria das pessoas as manifestações clínicas ocorrem na primeira infância.A persistência e a gravidade neste período antecipa persistência na juventude e na idade adulta, quando a remissão é incomum.Intervenção precoce pode romper este mecanismo e discute-se o papel que representam a alimentação materna e infantil, a exposição aos alérgenos da fumaça do cigarro, a exposição a alérgenos do ambiente doméstico, as infecções, bem como os mecanismos de intervenção precoce.
Método: Análise crítica e objetiva da literatura médica, obtida por pesquisa da MEDLINE, com revisão das influências sobre as patologias alérgicas mais comuns e do mecanismo de revertê-las.
Resultados: A combinação das exposições ambientais e as vulnerabilidades biológicas provem o milieu das causas das doenças alérgicas.O controle deste milieu com intervenções na alimentação materna e infantil, no ambiente domiciliar, nas infecções virais, na exposição à fumaça do cigarro, é um mecanismo eficiente de manipular o Th-2 no balanço Th-1/Th-2 para menos alergias bem como o estímulo do Th-1 com endotoxinas bacterianas, probióticos ou imunoterapia específica, pode diminuir a prevalência das doenças alérgicas.
Conclusões: A marcha atópica da criança alérgica pode ser interrompida por intervenções precoces na alimentação, no modo de vida, nas exposições ambientais.Estas intervenções visam interromper a seleção clonal de Th-2 que perpetua estas doenças.É possível também intervir com estímulo específico para expandir clonalmente o Th-1, que contrabalança o Th-2, com imunoterapia e com endotoxina bacteriana. A intervenção secundária e terciária com farmacoterapia é também importante no controle destas doenças ou contra a evolução para fases crônicas.
Early intervention in allergic diseases in pediatrics.
How and when
Abstract
Objective: Epidemiological and natural studies of allergic diseases have found that, for most people, clinical manifestations occur in early childhood. Both persistence and severity during early childhood predict disease persistence into later childhood and adulthood, at which point remission is uncommon. Early intervention might disrupt this mechanism and in discussion is the importance of maternal and child foods, exposition to allergens of the tobacco smoke, exposition to allergens of the domestic environment, infections, as well as the mechanism of early intervention.
Methods: Critical and objective analysis of medical literature using MEDLINE, with a review of the influences on the common allergic pathogies and the mechanism to overcome them.
Results: The combination of environmental exposures and biologic vulnerabilities provides a milieu for the allergic pathologies. To control this milieu with intervention in maternal and infant feeding, domestic environment, viral infections, exposition to tobacco smoke, is an efficient mechanism to manipulate the Th-2 in the Th-1/Th-2 balance toward less allergies as well as the stimulation of the Th-1 with bacterial endotoxins, probiotics or specific immunotherapy might reduce the prevalence of allergic diseases.
Conclusions: The atopic march of the allergic child could be interrupted by early interventions in feeding, life styling, and environmental exposition. These interventions try to disrupt the clonal selection of the Th-2 that turns on those diseases. It is possible as well the intervention with specific stimulation for clonal selection of the Th-1 with disbalance for the Th-2, mainly with immunotherapy and bacterial endotoxins.The secondary and tertiary interventions with farmacotherapy is also important in the control of these pathologies or against the evolution for chronic stages.
La intervención precoz en las doenças alérgicas en pediatría. Cómo e cuándo
Resumen:
Objetivo: Estudios epidemiológicos y de la historia natural de las enfermedades alérgicas han encontrado que en la mayor parte de las personas las manifestaciones clínicas ocurren en la primera infancia. La persistencia y la gravedad en ese periodo anticipa la persistencia durante la juventud y en el estado adulto, cuando la remisión no es común. La intervención precoz puede romper este mecanismo. Se discute el papel que representan la alimentación materna y la infantil, la exposición a los elementos alérgicos del humo de los cigarrillos, la exposición a los elementos alérgicos del ambiente doméstico y las infecciones, como también el papel de los mecanismos de la intervención precoz.
Método: Análisis critico y objetivo de la literatura médica, obtenida de la investigación realizada a través de MEDLINE, revisando las influencias sobre las patologías alérgicas más comunes y los mecanismos para revertirlas.
Resultados: La combinación de las exposiciones ambientales y las vulnerabilidades biológicas proveen el milieu de las causas de las enfermedades alérgicas. El control de este milieu, con intervenciones en la alimentación materna e infantil, en el ambiente domestico, en las infecciones virales, en la exposición al humo del cigarrillo y un mecanismo eficiente en la manipulación del Th-2, en el equilibrio Th-1/Th-2 para que se produzcan menor cantidad de alergias como también el estímulo del Th-1, utilizándose endotoxinas bacterianas, probióticos o inmunoterapia específica, lo que puede reducir el predominio de las enfermedades alérgicas.
Conclusiones: El curso atópico en el niño alérgico puede interrumpirse a través de intervenciones precoces en la alimentación, en el modus vivendi y en las exposiciones ambientales. Estas intervenciones tienen como objeto interrumpir la selección clonal de Th-2, que perpetua estas enfermedades. También es posible intervenir por medio de un estímulo específico para expandir clonalmente el Th-1, que contrabalancea el Th-2, con inmunoterapia y con endotoxina bacteriana. La intervención secundaria y terciaria con farmacoterapia también es importante para el control de estas enfermedades o contra su evolución hacia fases crónicas.
Introdução
As doenças alérgicas se manifestam em diferentes idades da infância e são principalmente a dermatite atópica, rinite alérgica, sibilação ou asma.
A dermatite atópica e a sibilação são mais comumente identificadas antes dos 2 anos de idade.A rinite alérgica e a asma são mais comuns após os 6 anos e principalmente após os 11 anos.O mais interessante é que estas patologias são inter-relacionadas, ou seja, a presença de dermatite atópica é associada com grande risco de asma mais tarde, no que se convencionou chamar de marcha atópica, pela qual quando uma diminui a outra aumenta.
O aumento destas doenças alérgicas que até 1970 acometia 10% da população e hoje acomete 30 a 35%, não pode ser explicado apenas pelo fator genético ou familiar, embora este tenha grande importância1.Um estudo em 1998 com 306 crianças de 1 a 24 anos de idade com história de asma na família concluiu que asma materna era maior indicador de asma futura na criança do que a presença de asma paterna2.Estes achados sugerem que a doença alérgica na mãe é maior fator de risco para a criança e os possíveis mecanismos de transferência seriam transferência transplacental, anticorpos maternos ou citocinas maternas.Alguns estudos sugerem também que a exposição materna a alérgenos no útero pode influenciar a criança a responder precocemente3,4.Outros fatores tais como alimentação materna e na primeira infância, endotoxinas bacterianas, exposição a produtos químicos oriundos do tabagismo materno intra-útero ou nos primeiros anos de vida e infecções virais são também apontados5-8.
O outro grande motivo apontado para o aumento das alergias tem sido o maior conforto dos lares; cada vez mais as crianças passam maior tempo dentro dos lares e cada vez mais aumentam os reservatórios domiciliares para alérgenos, principalmente os ácaros domiciliares, pelos de animais, fungos e restos de barata que aumentam a exposição e a sensibilização das crianças a estes alérgenos9-11.Esta sensibilização aos alérgenos ambientais ocorre principalmente entre 1 e 2 anos de idade12, embora algumas sensibilizações já possam ocorrer dentro do útero materno a partir dos seis meses de gestação, p.e. foi demonstrada sensibilização de células mononucleares do feto com resposta imunoproliferativa a estes alérgenos, indicando que desvio de Th-2 para doenças alérgicas está presente neste nível antes do nascimento13.Este fato merece destaque, pois as prevenções de atopias devem iniciar na maternidade, continuar nos primeiros anos de vida e posteriormente durante o crescimento da criança.
Importância do pré-natal nas doenças alérgicas
Como foi demonstrado, a história familiar e principalmente a materna, tem grande influência no desenvolvimento das alergias.Sabe-se que um comportamento Th-2 placentário é importante para a sobrevivência do feto e portanto está presente no útero14. Desta maneira, ao nascimento, existe um padrão de resposta Th-2 que é associado com citocinas pró-inflamatórias características de indutoras de IgE e eosinofilia tecidual, padrão de doenças alérgicas, que são a IL-4, IL-5, IL-6, IL-9, IL-10 e IL-1315.Existem inúmeros estudos que ligam a produção destas citocinas com o futuro desenvolvimento de alergias 16,17.Como baixos níveis de INF-g em adultos estão relacionados com doença alérgica, a baixa desta citocina é considerada um marcador de patologia alérgica.Para investigar esta correlação foi realizado um estudo no cordão umbilical de 35 recém natos e eles foram acompanhados por 1 ano.O resultado mostrou que as crianças exibindo doença atópica e também testes cutâneos positivos a alérgenos, apresentavam muito menos INF-g no nascimento, quando comparadas às crianças não atópicas 18.
Desta maneira é importante que no pré-natal seja necessário educar e orientar a mãe alérgica em diminuir ao máximo a exposição alergênica na gravidez para não gerar filhos mais alérgicos.Embora seja assunto em discussão, parece que evitar que a criança atópica se alimente de leite de vaca ou cabra e deixa-la amamentar o maior tempo possível ao seio materno diminui o risco de desenvolver doença alérgica9.
A exposição aos alérgenos na infância
Após o nascimento, a maturação do sistema imunológico é caracterizada por um desenvolvimento balanceado do Th-1/Th-2; a eficiência e a cinética deste processo é determinada hereditariamente, mas pode ser influenciada consideravelmente pelo meio ambiente em que a criança nasce19.Normalmente o padrão Th-2 é característico ao nascimento, mas nos primeiros anos de vida a resposta vai sendo paulatinamente modificada com o aumento do padrão Th-1. Este desvio de padrão ocorre primeiro para os antígenos alimentares e depois para os inalantes e é muito mais rápido nos não atópicos do que nos atópicos.No entanto o padrão Th-2 característico dos alérgicos, pode aumentar muito nos primeiros anos devido à exposição da criança ao meio ambiente, a alimentação, as infecções por vírus, a fumaça de cigarro e esta resposta pode ser intensificada pela re-exposição ao mesmo alérgeno por um padrão polarizado da resposta imune20.Um estudo importante neste aspecto relacionou a exposição da criança ao alérgeno de ácaro(Der p 1) e o desenvolvimento de sensibilização atópica21.Havia uma tendência de dose-resposta entre exposição e grau de sensibilização com 1 ano de idade.Também se detectou associação entre sensibilização ao Der p 1 e asma aos 11 anos de idade.A maioria das crianças asmáticas aos 11 anos tinha sido exposta a níveis superiores a 10 mg/g de poeira durante a infância.O risco relativo de desenvolver asma aos 11 anos nas crianças sensibilizadas ao Der p 1 foi de 5.3(95% CI, 2.3-12.6)21.Outros estudos também investigaram esta relação de exposição e sibilos freqüentes logo nos dois primeiros anos de vida, sibilos estes que são uma das manifestações iniciais da asma22.
Outros estudos encontraram relação entre níveis de exposição a alérgeno de barata(Bla g 1 ou 2)na casa e sibilos no primeiro ano de vida.O risco relativo de sibilância nas crianças expostas a no mínimo 0.05 mg/Bla g 1 ou 2 foi de 1.63(95% CI, 1.05-2.55)22.
O efeito de exposição a animais domésticos, tais como o cão e o gato, no desenvolvimento de doenças alérgicas apresenta resultados controversos; alguns estudos mostram claramente a relação de exposição ao cão e sensibilização com IgE específica e doença alérgica mais tarde na criança23,24, enquanto outros demonstram, ao contrário, efeito protetor25,26, e até mesmo demonstram que a remoção do cão é relacionada à diminuição do efeito protetor 27.
Estudos prospectivos indicam que níveis baixos de alérgeno de gato são associados com risco de sensibilização e parece haver associação entre dose de exposição e resposta, pelo menos nos primeiros anos de vida28.Já aquelas crianças expostas a altos níveis de alérgeno de gato podem inicialmente desenvolver uma resposta IgE, mas depois vão desenvolver uma resposta Th-2 modificada em forma de tolerância e produção de IgG e IgG4 predominante e que levará a uma diminuição do risco de asma na infância29,30.
Tabagismo materno durante a gestação e nos primeiros de vida da criança está correlacionado com aumento de asma, devendo a intervenção precoce atingir a mãe durante a gestação27.
Vários estudos prospectivos de prevenção primária de alergias e asma foram realizados e concluem que redução de alérgenos do ambiente desde o nascimento e nos primeiros anos da criança são da maior importância para se evitar o aparecimento de doenças alérgicas mais tarde28,31,32.Em trabalhos anteriores temos demonstrado que, mesmo na doença alérgica instalada, é possível melhorar os sintomas e o consumo de medicamentos dos alérgicos somente com medidas de controle ambiental que diminuem os alérgenos do ambiente domiciliar 33-35.
A exposição aos micróbios e vírus na infância
Da mesma maneira que exposição alergênica, a exposição precoce aos micróbios e vírus pode alterar o risco para o desenvolvimento de doenças alérgicas.
Em crianças de até 6 anos de idade as infecções por vírus parainfluenza e sincicial respiratório estão relacionados com o aumento de asma mais tarde, embora estes vírus não tenham influência quando acometem crianças maiores de 6 anos de idade36.
Vírus comuns dos resfriados quando acometem crianças de baixa idade estão correlacionados com menor risco de asma após os 7 anos37, parecendo haver um efeito protetor e explicando porque as crianças que crescem em grandes famílias junto a outras crianças, ou que são criadas em creches, são menos propensas a desenvolverem asma mais tarde a partir dos 11 anos de idade37.
Em contraste com os estudos apresentados em relação à exposição alergênica, que mostram risco de aumento das atopias, a exposição precoce a micróbios ou infecção microbiana, podem atualmente conferir proteção contra o desenvolvimento de doenças alérgicas mais tarde.A infecção na mãe durante a gestação pode aumentar o risco de atopia na criança, mas muitas evidências existem de que estas infecções na infância podem conferir proteção.O famoso estudo Tucson Children’s Respiratory Study de Martinez e cols mostra claramente isto quando acompanhou crianças de 6 a 13 anos de idade que freqüentavam o mesmo maternal e escola37.Outro estudo importante acompanhou crianças de 6 a 13 anos de idade e verificou a importância de exposição ao meio rural precoce na infância e desenvolvimento de doença alérgica mais tarde.A prevalência de atopia foi significantemente menor entre crianças que estavam expostas a estábulos para a criação de gado e uso de leite ao pé da vaca(não pasteurizado) no primeiro ano de vida, quando comparadas às crianças urbanas que não estavam expostas a estas condições(1% vs 12% respectivamente, com p
Outro assunto interessante a este nível é a hipótese do uso de probióticos na prevenção de doenças atópicas.O uso de lactobacillusoral pode estimular a flora intestinal a criar mecanismo de desenvolvimento imunológico que previne atopias.Um estudo interessante publicado no Lancet em 200141 mostra que 155 mães atópicas receberam lactobacillus CG, bem como os filhos gerados receberam por 6 meses e foram avaliados aos 2 anos de idade, concluindo-se por redução de 50% de incidência de dermatite atópica nas crianças tratadas, comparadas às não tratadas.
A intervenção precoce com medicamentos para as doenças alérgicas
Os corticóides inalados são atualmente considerados de primeira linha no tratamento da asma em pacientes com sintomas persistentes e têm sido preconizados naqueles com sintomas intermitentes42.O reconhecimento de que a asma é uma doença fundamentalmente inflamatória crônica tem sugerido a utilização dos CI em fases cada vez mais precoces e vários estudos demonstram que pacientes com asma leve são tratados de modo insuficiente e podem evoluir para um remodelamento da árvore respiratória, justificando tal intervenção precoce43.Outros estudos documentam menor efeito do corticóide inalado sobre a asma quando instituídos muitos anos após a sua instalação44.
O estudo CAMP(Childhood Asthma Management Program) utiliza CI em crianças de 5 a 12 anos com asma leve a moderada e por 5 anos e documenta uma melhora acentuada quando comparadas com um grupo usando nedocromil ou placebo.Além disto demonstra uma queda nas provas de broncoprovocação 4 meses após a descontinuação do CI, evidenciando a hipótese de que os melhores resultados ocorrem naquelas terapias que se iniciam logo na instalação da asma45.O estudo PEAK(Prevention of Early Asthma in Kids) que estuda o efeito de CI em crianças de 2 a 4 anos de idade e durante 2 anos, suporta esta afirmativa e está em andamento nos USA.Todos estes estudos enfocam a precocidade do uso dos CI para não somente o controle da doença crônica em qualquer nível, mas também para se evitar o remodelamento da árvore brônquica que implica em espessamento irreversível da membrana basal com hipertrofia e hiperplasia da musculatura lisa limitando o fluxo aéreo.Até mesmo o uso de CI não por via oral, mas por via nasal, pode proteger contra exacerbações de asma, bem como pode reduzir a hiperreatividade brônquica e melhora dos sintomas clínicos asmáticos, evidenciando o conceito de que as intervenções nas vias aéreas superiores podem influenciar favoravelmente nas vias aéreas inferiores, de acordo com o postulado pelo ARIA Workshop Report(Allergic Rhinitis and Its Impact on Asthma), (Reis, AP et als-submetido à publicação).
Trabalhando no conceito da “marcha atópica” pelo qual criança com dermatite atópica deverá manifestar asma mais tarde, o estudo ETAC(Early Treatment of the Allergic Child) testou esta hipótese usando o antihistamínico cetirizina em 566 crianças com 1 a 2 anos de idade e por 18 meses, e ainda acompanhamento por outros 18 meses e concluiu por 50% menos incidência de asma nestes períodos, quando comparadas com o grupo controle46.Em 1987 nós mesmos já citávamos esta perspectiva do uso preventivo dos antihistamínicos em asma brônquica induzida por exercício 47.
Os antileucotrienos montelukaste(para crianças acima de 2 anos) e zafirlucaste(para crianças acima de 6 anos) são terapia alternativa para tratamento de asma e podem ser combinados com o uso dos corticóides inalados na asma persistente moderada.Têm sido usados também em bronquiolites por vírus sincicial respiratório a fim de se evitar o desenvolvimento de alterações crônicas após a infecção viral 48.
A intervenção precoce com alérgenos em imunoterapia
De acordo com a Organização Mundial de Saúde, a imunoterapia com os mesmos alérgenos sensibilizantes pode reduzir os sintomas de rinite alérgica e asma brônquica, quando comparados com o placebo49.A imunoterapia específica com alérgenos pode ter efeito imunomodulatório e se associa com aumento de expressão de INF-g na mucosa estimulada pelo alérgeno, sugerindo que a IT promove estímulo do Th-1 e diminuição dos efeitos das citocinas Th-2, resultando na supressão de imunoglobulina IgE e dos eosinófilos, que se constituem na expressão das alergias50.Tem sido também demonstrado que a IT precoce e antes dos 3 anos de idade leva a mudanças do padrão imunológico de Th-2 para Th-1, podendo daí mudar o curso natural da doença alérgica, o que nenhuma das outras intervenções pode fazer51.O estudo multicêntrico europeu PAT(Preventive Allergy Treatment Study) demonstrou que a IT por 2 anos em crianças com rinoconjuntivite alérgica pode reduzir o desenvolvimento de asma mais tarde52.Outros estudos recentes mostram também que IT em crianças monosensibilizadas pode prevenir a sensibilização adicional a outros alérgenos53.Outro fato importante e documentado é que, após descontinuar a IT e depois de 3 a 4 anos, se mostrou que as crianças permaneciam em remissão clínica da patologia alérgica ainda por pelo menos 3 anos54.É necessário assinalar que todos estes trabalhos se referem a imunoterapia por via injetável e que, embora a WHO(World Health Organization) tenha em 1998 firmado uma posição contrária a imunoterapia via oral, o ARIA-200155 concluiu, quando analisa os efeitos da imunoterapia, que a IT local mas com altas doses de alérgenos específicos, e não os coquetéis de baixas doses existentes no mercado brasileiro, podem ser indicados pelas vias nasal ou sublingual abrindo agora uma perspectiva para este tipo de tratamento em crianças.Os problemas nesta terapia são os altos custos envolvidos na purificação destes antígenos e em altas doses.
Fato recente e interessante de assinalar é a tentativa de se combinar a imunoterapia específica e o uso de anticorpo monoclonal anti-IgE(omalizumab) no tratamento de certos casos complexos de alergias em pediatria.Estudo duplo cego e controlado em 221 crianças de 6 a 17 anos de idade, portadoras de rinoconjuntivite alérgica sazonal, receberam esta terapia que reduziu em 48% os sintomas clínicos e o uso de terapia de resgate quando comparada ao grupo controle que recebeu apenas IT56.
Conclusões
A dermatite atópica, a sibilância infantil, a rinite alérgica e a asma brônquica são doenças alérgicas inter relacionadas e são componentes da marcha atópica.Intervir e precocemente é obrigação do médico pediatra pois somente assim poderá se evitar a evolução desfavorável e o agravamento destas patologias.A história familiar e principalmente a materna, até que tenhamos um mapeamento genético prático, parece ser um dos indicativos mais fortes de praticarmos esta intervenção, que deve ser iniciada na mãe e continuada principalmente nos primeiros anos de vida.Embora não existam condições de se alterar o genoma da criança alérgica, podemos intervir no segundo componente da marcha natural e podemos prevenir e até alterar este curso.Evitar que a mãe use cigarro na gestação e evitar fumar na presença da criança recém nascida e amamentar ao seio o maior tempo possível é política importante.Evitar introduzir leite de vaca ou cabra no primeiro ano de vida do atópico e controlar os alérgenos domiciliares a que a mãe atópica e a criança estão expostas, e principalmente ácaros, fungos, pelos de animais e baratas, parece ser importante para se evitar a sensibilização e o desenvolvimento da doença alérgica.Ao contrário, pode ser que deixá-la exposta a endotoxinas bacterianas e mesmo a algumas infecções virais sem gravidade, pode ser um bom caminho de se prover defesa imunológica a estas crianças.O uso de medicamentos precocemente para reduzir a evolução e mesmo o agravamento destas doenças é também atitude que se exige do pediatra moderno.A imunoterapia precoce pode até mesmo alterar o curso natural da doença alérgica e, conjuntamente com as outras medidas preventivas, parece ser o caminho atual para prover as crianças atópicas de menor sofrimento futuro.
CONSENSO BRASILEIRO SOBRE ALERGIA ALIMENTAR 2007 Rev. Bras.Alerg.Imunopatol 2008; 31:No. 2
Food Allergy: A practice parameter updated-2014- JACI 134:5;1016-1025
Allergy 2008: 63: 793–796 Testing for IgG4 against foods is not recommended as a diagnostic
tool: EAACI Task Force Report
Consultoria de Dr Ataualpa P. Reis, médico alergista e imunologista e do Conselho Científico da ASBAI MG
“Asma e alergias: é preciso cuidar do ambiente"
As alergias atingem de 30 a 35% dos brasileiros e resultam de uma combinação da bagagem genética individual, que torna o organismo de algumas pessoas mais sensível, com fatores agressivos presentes no ambiente, chamados alérgenos. Os mais comuns estão dentro do próprio domicílio. São os ácaros encontrados na poeira, restos e fezes de baratas, mofo, pêlos de animais domésticos, fumaça de cigarro, pólen e esporos de fungos, além de certos alimentos, medicamentos e produtos químicos. Os alérgenos podem causar danos à saúde provocando alergias e doenças como a asma.
Segundo Reis, quando uma pessoa alérgica entra em contato com algum desses agentes alérgenos, seu sistema de defesa reage de forma exagerada, produzindo os sintomas das alergias, entre eles, os das alergias respiratórias, que incluem espirros constantes, coriza, sensação de nariz entupido ou de “cabeça pesada” e coceira nos olhos, no nariz, no céu da boca e na garganta. “Já nas crises de asma, os pacientes têm ‘chiado’, tosse, falta de ar, sensação de ‘aperto’ no peito e cansaço. O incômodo é maior sobretudo à noite ou ao acordar e tende a piorar com esforço físico”, explica.
A asma brônquica é uma das doenças alérgicas mais preocupantes já que atinge uma de cada quatro crianças na faixa dos seis aos 14 anos, conforme um estudo internacional concluído em 1998 e confirmado em 2003 e 2006 com publicação internacional na revista científica Lancet. Os casos mais graves geram 370 mil internações por ano no País e gastos da ordem de R$ 76 milhões de dólares para o Sistema Único de Saúde (SUS), conforme dados do Datasus-2003. Sem contar que a mortalidade por asma dobrou nos últimos 30 anos e alcança hoje seis mortes notificadas por dia, revela o Datasus.
O alergologista orienta que uma das principais formas de deter as crises é fazer o tratamento preventivo medicamentoso, sob orientação médica. “Outro cuidado fundamental é manter os ambientes limpos, livres de ácaros e poeira”. Ele sugere que a pessoa encape colchões e travesseiros com tecidos impermeáveis; use pano úmido e produtos que eliminem o mofo no chão e nas paredes; remova tapetes, cortinas e bichinhos de pelúcia; deixe os ambientes ventilados e iluminados pelo sol. Medidas como eliminar o cigarro dos ambientes fechados e fumar longe das crianças também são importantes.
Para prevenir as alergias respiratórias e a asma
· Manter os ambientes secos e abertos, permitindo a circulação do ar e a entrada dos raios de sol, capazes de destruir os ácaros;
· Incentivar as crianças a brincar ao ar livre, agasalhando-as no tempo de frio;
· Encapar colchões, travesseiros e almofadas com plástico ou tecidos impermeáveis;
· Trocar a roupa de cama pelo menos uma vez por semana, lavando-a em água quente;
· Usar cobertores antialérgicos, lavando-os regularmente e deixando ao sol para secar;
· Evitar plantas, animais de estimação, bichinhos de pelúcia, tapetes ou carpetes, livros e brinquedos acumulados no quarto das crianças;
· Retirar as cortinas ou usar aquelas de tecido sintético, mais finas, curtas e presas por argolas para facilitar a remoção e a lavagem a cada 15 dias;
· Substituir a vassoura por pano úmido na limpeza diária, afastando as pessoas alérgicas;
· Aplicar produtos antimofo e acaricidas em carpetes, frestas e cantos dos móveis;
· Não usar inseticidas em spray nem espiral;
· Jamais fumar dentro de casa, perto de crianças ou mesmo de adultos alérgicos.
Fonte: Sociedade Brasileira de Alergia e Imunopatologia – Regional Minas Gerais
Dados epidemiológicos mais recentes demonstram que a prevalência das doenças alérgicas vem aumentando muito no mundo e no nosso país.Atualmente podemos afirmar que tais alergias acometem 35% da nossa população e que a asma brônquica alcança 25% ,segundo levantamento epidemiológico do estudo ISAAC(International Study of Asthma and Allergy in Children).
Algumas cidades têm prevalência maior que outras, sendo maiores em Recife e Porto Alegre e menores em Itabira-MG.
A morbidade da asma é grande e é a segunda causa de internações hospitalares no Brasil, com gastos de milhões de reais pelo SUS (350.000 internações e gastos de 76 milhões de reais no levantamento de 1996).Também a mortalidade vem aumentando, sendo que no período de 1970 a 1996 dobrou (subiu de 0.3/100.000 habitantes para 0.6 por 100 mil).
A mudança climática, própria do período de inverno, traz consigo condições ideais para o reaparecimento das infecções viróticas e das alergias.
É necessário distinguir bem os resfriados das gripes e das crises alérgicas e cuidar-se.
Os resfriados são infecções viróticas mais leves e provocadas principalmente pelos rinovírus e adenovírus.Os sintomas que aparecem são de dor de cabeça, nariz entupido, dor de garganta, tosse seca, fadiga geral e febre baixa e duram em média uma semana.Já a gripe é provocada por vírus mais fortes (influenza, vírus sincicial, adenovirus, etc)e a infecção adquire caráter mais sério com febre alta, aumento de gânglios, tosse com secreção, dores fortes no corpo.O resfriado comum pode também se complicar com infecção bacteriana e apresentar os mesmos sintomas.Geralmente estas infecções representam uma sinusite, otite, bronquite ou pneumonia.
Ao contrario do que as pessoas acreditam, infecções por vírus se contrai principalmente através das mãos e menos por contato com espirros ou tosse de pessoas doentes.O vírus fica 3 horas vivo nas mãos que são levadas ao telefone, maçanetas, etc, e o individuo se contamina por dar as mãos ou pegar nas superfícies onde estão os vírus e leva a boca, nariz ou olhos e está completado o ciclo de contaminação.
Prevenir-se evitando dar as mãos para cumprimentar e lavando sempre as mãos para retirar os vírus é bastante recomendável.Também aglomerações são fontes de contaminação.
Uso de vitamina C em altas doses (seis grs ao dia) e por dois a três dias no início do processo e analgésicos-antitérmicos é advogado por vários médicos (existem contradições) como método eficaz de tratamento.As gripes e infecções secundárias exigem que você consulte o seu médico que pode avaliar a extensão e necessidade de uso de outros medicamentos (inclusive antibióticos (nunca os use por conta própria e por poucos dias-antibióticos não são eficazes contra vírus)).
Existe uma vacina antigripe do Instituto Pasteur e de outros, comercializada no Brasil e que protege em 70% das infecções viróticas e por um ano.São indicadas para pessoas idosas, fracas ou sujeitas a infecções repetitivas.Há tendência hoje de se vacinar crianças asmáticas pequenas, pois os vírus respiratórios têm influência no desenvolvimento e piora da asma.
As crises alérgicas se intensificam devido às modificações climáticas que diminuem as secreções e as defesas.Diferencia-se das infecções por não provocarem sintomas gerais e não debilitarem o organismo.Ocorrem os anos todo e apenas se intensificam neste período.Aumentam também pelo fato das pessoas tenderem a ficar mais tempo dentro de ambientes fechados e se aglomerarem mais.
Existe uma concordância internacional de que as alergias estão intimamente relacionadas à poluição do ambiente em que a pessoa vive e que este ambiente pode ser relativamente bem controlado, diminuindo a incidência da doença alérgica, conforme trabalho científico desenvolvido em Minas Gerais e apresentado no último Congresso da Academia Americana de Alergia Asma e Imunologia. Algumas recomendações são básicas, tais como encapar com pano impermeável os colchões e travesseiros que são reservatórios do principal causador das alergias respiratórias e que são os ácaros.Também deixar entrar sol no ambiente, pois este é acaricida e aplicar produtos antiácaros, antimôfos ou desnaturantes de proteínas, alem de limpar o ambiente com pano úmido.
Ataualpa P. Reis-Membro da Sociedade Brasileira de Alergia e Imunopatologia
Nas Doenças Respiratórias, principalmente na Asma que ocorre em 10% da população adulta e 25% na infantil, estamos atualmente personalizando o diagnóstico com informações precisas das causas alérgicas, com testes moleculares por técnicas de microarrays, biomarcadores capazes de individualizar o tipo causal da Asma, identificando fenótipos e endotipos e levando a uma medicina personalizada inexistente anteriormente. Por consequência, o tratamento também fica personalizado e já usamos os imunobiológicos que são montados por engenharia genética em laboratório e são bloqueadores da resposta imunológica existente na Asma, constituindo hoje medicina de ponta ( omalizumabe, mepolizumabe, benralizumabe, dupilumabe e outros em desenvolvimento). Por último, a epigenética que aumentou muito o conhecimento do mecanismo genético da Asma e que torna possível, em muito em breve, controlar o desenvolvimento da Asma e até mesmo impedir que ela se desenvolva, silenciando os genes predisponentes que levariam uma pessoa a desenvolver a Asma. Portanto, e por todos estes motivos, pode-se dizer que estamos entrando na era da cura da Asma.
Takaro TK, Krieger J, Song L, Sharify D, Beaudet N. The Breathe-Easy Home: the impact of asthma-friendly home construction on clinical outcomes and trigger exposure. Am J Public Health. 2011 Jan;101(1):55-62.
OBJECTIVES: We examined the asthma-control benefit of moving into an asthma-friendly Breathe-Easy home (BEH).
METHODS: We used a quasi-experimental design to compare the asthma outcomes of 2 groups of low-income children and adolescents with asthma: 34 participants who moved into a BEH, and a local matched cohort of 68 participants who had received a previous asthma-control intervention. Both groups received in-home asthma education. BEHs were constructed with moisture-reduction features, enhanced ventilation systems, and materials that minimized dust and off-gassing.
RESULTS: BEH residents' asthma-symptom-free days increased from a mean of 8.6 per 2 weeks in their old home to 12.4 after 1 year in the BEH. The proportion of BEH residents with an urgent asthma-related clinical visit in the previous 3 months decreased from 62% to 21%. BEH caretakers' quality of life increased significantly. The BEH group improved more than did the comparison group, but most differences in improvements were not significant. Exposures to mold, rodents, and moisture were reduced significantly in BEHs.
CONCLUSIONS: Children and adolescents with asthma who moved into an asthma-friendly home experienced large decreases in asthma morbidity and trigger exposure.
A casa fácil de respirar: o impacto da construção da construção de uma casa favorável à asma sobre os desfechos clínicos e a exposição provocada
Takaro TK, Krieger J, Song L, Sharify D, Beaudet N. The Breathe-Easy Home: the impact of asthma-friendly home construction on clinical outcomes and trigger exposure. Am J Public Health. 2011 Jan;101(1):55-62.
OBJETIVOS: Foi examinado o benefício sobre o controle da asma da mudança para uma casa fácil de respirar, favorável à asma.
MÉTODOS: Foi utilizado um desenho quase experimental para comparar os desfechos da asma de 2 grupos de crianças e adolescentes asmáticos com baixa renda: 34 participantes que se mudaram para uma casa fácil de respirar e uma coorte de 68 participantes que receberam intervenção prévia para o controle da asma. Ambos os grupos receberam educação domiciliar sobre a asma. As casas fáceis de respirar foram construídas em cenários com redução de umidade, melhora dos sistemas de ventilação e materiais que minimizam poeira e escape de gases.
RESULTADOS: O número de dias livres de sintomas aumentou de uma média de 8,6 por 2 semanas na casa antiga para 12,4, após 1 ano na casa fácil de respirar. A proporção de moradores da casa fácil de respirar com uma consulta clínica de urgência relacionada à asma nos últimos 3 meses reduziu de 62% para 21%. A qualidade de vida dos cuidadores aumentou significativamente. O grupo da casa fácil de respirar melhorou mais do que o grupo de comparação, mas a maioria das diferenças não foram significativas. As exposições a mofo, roedores e umidade reduziram significativamente nas casas fáceis de respirar.
CONCLUSÕES: Crianças e adolescentes com asma que se mudam para uma casa favorável à asma experimentam grandes decréscimos na morbidade da asma e na exposição provocada.
COMENTÁRIOS de ATAUALPA P.REIS
O trabalho de Takaro e colaboradores reforça o conceito da necessidade de controle do ambiente em que se vive e asma 1,2,3. Não somente os 34 participantes do projeto de mudá-los para uma casa boa para se respirar se beneficiaram com o número de dias livres de sintomas, aumentando de uma média de 8,6 por 2 semanas na casa antiga para 12,4, após 1 ano na casa fácil de respirar , com a proporção de moradores da casa fácil de respirar com uma consulta clínica de urgência relacionada à asma nos últimos 3 meses reduzindo de 62% para 21%; como também se beneficiaram os controles de uma coorte de 68 participantes que também foram submetidos a um programa em que receberam intervenção prévia para o controle da asma.
Alguns trabalhos recentes avaliaram individualmente cada uma da condutas de controlar os alérgenos do ambiente e concluíram pela ineficácia da conduta do ponto de vista clínico4,5,6, embora trabalhos de controle global tenham demonstrado eficácia7,8,9, e,assim, este trabalho é importante para esclarecer a questão da casa com boa qualidade para respirar em que as exposições a mofo, roedores e umidade reduziram significativamente.
REFERÊNCIAS:
1 - Burr ML,Mathews IP,Arthur RA et al. Effects on patients with asthma of eradicating visible indoor mold: a randomized controlled trial 2007-Thorax;62:767-72
2 - Kattan M, Stearns SC, Crain EF et al. Cost-effectiveness of a home-based environmental intervention for inner-city children with asthma. 2005 J Allergy Clin Immunol;116:1058-63
3 - Krieger JW, Takaro TK, Song L et al. The Seattle-King count health homes project: a randomized controlled trial of a community health worker intervention to decrease exposure to indoor asthma triggers. Am J Public Health 2005;95:652-59
4 - MacKeever K. Dust mites trump asthma prevention guidelines: study finds that despite heroic efforts, most strategies are doomed to fail. 2008; available at: http//www.hon.ch/news/HSN/614473.htm
5 - Dust mite control measures of no use. Editorial Lancet 2008;371:1390
6 - Gotzsche PC. Asthma guidelines on house dust mites are not-evidence-based. 2007;Lancet 370:2100-1
7 - Platts Mills TAE, Vaughan JW, Carter MC. The role of intervention in established allergy: avoidance of indoors allergens in the treatment of chronic allergic diseases. J Allergy Clin Immunol 2000; 106:787-804
8 - Morgan WJ, Crain EF, Gruchalla RS, O´Connor GT, Kattan M, Evans R et al. Results of a home-based environmental intervention among urban children with asthma. N Engl J Med 2004;351:1068-80
9 - Platts-Mills TAE. Allergen avoidance in the treatment of asthma: problems with the meta-analyses. J Allergy Clin Immunol 122:694-96.
Medicina Atual Pediatria Ginecologia Oncologia
ISSN 1519-521X - Volume 16 - Nº 4
1 - Qual a definição de DPOC?
Doença pulmonar obstrutiva crônica (DPOC) é uma doença comum, evitável e tratável, caracterizada por limitação persistente do fluxo aéreo, usualmente progressiva, associada a um aumento da resposta inflamatória crônica nas vias aéreas e nos pulmões à exposição de partículas ou gases nocivos (Global Initiative for Obstructive Lung Disease, 2015).
As definições atuais de DPOC não fazem referência aos termos bronquite crônica e enfisema, embora a inflamação nas pequenas vias aéreas (bronquite e bronquiolite crônicas) e a destruição do parênquima pulmonar (enfisema) sejam as anormalidades anátomo-patológicas que determinam a obstrução ao fluxo aéreo. A contribuição de cada componente na patogênese da DPOC varia de paciente para paciente.
2 - O que é bronquite crônica?
Bronquite crônica é uma condição clínica definida pela presença de tosse e produção de escarro por pelo menos 3 meses em 2 anos consecutivos. Ela pode existir antes da presença da obstrução ao fluxo aéreo e quando esta surge caracterizamos a presença de DPOC.
3 - O que é enfisema pulmonar?
Enfisema pulmonar é definido anatomicamente como um alargamento anormal e permanente dos espaços aéreos distais ao bronquíolo terminal, acompanhado de destruição de suas paredes, sem fibrose óbvia. Em termos fisiopatológicos, a inflamação existente na DPOC, juntamente com participação do estresse oxidativo e do desequilíbrio entre proteases e antiproteases, leva à destruição da parede alveolar e à consequente perda dos pontos de fixação das vias aéreas terminais aos alvéolos, com colapso expiratório dos mesmos, limitação do fluxo aéreo e hiperinsuflação pulmonar.
4 - Como pode ser definida a DPOC do ponto de vista clínico?
Do ponto de vista clínico podemos usar uma definição de trabalho de DPOC como sendo uma condição pulmonar crônica, caracterizada pela presença de tosse produtiva e/ou dispneia aos esforços, geralmente progressiva, determinada na maioria das vezes pela exposição à fumaça do cigarro ou, eventualmente, a outras substâncias inaladas.
No início da doença, os sintomas não são constantes e são geralmente de baixa intensidade, mas intensificações dos mesmos podem ocorrer em intervalos variáveis, principalmente nos meses frios e em casos de infecções respiratórias, caracterizando as exacerbações. Com o progredir da doença os sintomas ficam mais intensos e as exacerbações, mais comuns.
Capítulo 2 - Epidemiologia
5 - Qual o impacto epidemiológico da DPOC?
As estimativas da prevalência da DPOC dependem de quais critérios são utilizados para o seu diagnóstico. Como os mesmos não são precisos e são variados, é difícil quantificar a prevalência, morbidade e mortalidade desta doença. Quando se considera apenas o relato do próprio paciente de que tem o diagnóstico médico de DPOC, a prevalência é baixa, alguns estudos apontando para menos de 6%. Por outro lado, estudos que utilizam metodologia padronizada, incluindo espirometria, estimam que aproximadamente 25% dos adultos com idade acima de 40 anos têm algum grau de limitação ao fluxo aéreo.
Quanto à morbidade, a DPOC é uma doença que tradicionalmente acarreta aumento nas hospitalizações, atendimento nos serviços de urgência e consultas médicas, principalmente entre os pacientes em fases mais avançadas. Estudo europeu mostra que o número de consultas por DPOC é maior do que as visitas médicas por asma, pneumonia, câncer de pulmão e tuberculose. Nos EUA, em um único ano, a DPOC foi responsável por oito milhões de consultas médicas, 1,5 milhões de atendimentos em serviços de emergência e mais de 650 mil hospitalizações. No Brasil, mais de 150 mil hospitalizações por DPOC ocorrem anualmente, somente no serviço público de saúde.
Em relação à mortalidade, a OMS (Organização Mundial de Saúde) estima que a DPOC foi a sexta causa de morte no mundo em 1990, projetando-a como a terceira causa no ano de 2020 e a quarta em 2030. No Brasil, a DPOC é responsável por cerca de 30 mil óbitos por ano.
6 - O que foi o estudo PLATINO?
Foi um estudo multicêntrico, transversal de base populacional, criado para se avaliar a prevalência da DPOC e analisar o seu impacto nesta amostra. Foi realizado em cinco grandes cidades da América Latina (Projeto Platino - Proyecto Latinoamericano de Investigación em Obstrucción Pulmonar): São Paulo, Cidade do México, Montevidéu, Santiago e Caracas. O estudo constou de aplicação de questionários e espirometria pré e pós-broncodilatador em indivíduos com idade acima de 40 anos, vivendo em residências escolhidas de forma randômica. Foi utilizada como definição de DPOC a relação VEF1/CVF
7 - Qual o impacto epidemiológico da DPOC no Brasil?
Segundo o DataSUS (www.datasus.gov.br), a DPOC varia entre a 5a e a 7a causa de morte no Brasil. Em 2006 ela era 7a causa com 37.637 mortes, atrás das neoplasias (144.347 mortes), doenças cerebrovasculares (93.372 mortes), doenças isquêmicas do coração (88.092 mortes), outras doenças cardíacas (59.045), das causas externas (46.537 mortes) e do diabetes (43.744).
De acordo com os dados do SUS, mais de 125.000 hospitalizações por DPOC ocorreram no Brasil no ano de 2008, sendo mais frequentes nas regiões Sul e Centro-Oeste. Se considerarmos que 30% a 40% da população brasileira é atendida por seguros de saúde e supormos que eles também se internam na mesma proporção, devem ter ocorrido 250 mil internações neste período. Os valores destas internações, a preço de SUS, alcançaram mais 100 milhões de reais.
Capítulo 3 - Fisiopatologia
8 - Qual a etiologia da DPOC?
A DPOC é resultado da interação entre exposição a partículas e/ou gases nocivos e fatores genéticos e ambientais. Dentre as exposições, o tabagismo é a principal, sendo responsável por aproximadamente 95% dos casos. Outras formas de tabaco, como charuto e cachimbo, assim como o tabagismo passivo, também podem causar DPOC.
Outras exposições também se associam à DPOC:
- Ocupacionais: poeiras orgânicas e inorgânicas, fumaça, agentes químicos;
- Fumaça da queima de lenha;
-
Fumaça da queima do carvão.
9 - Quais as evidências sobre a predisposição genética na DPOC?
A predisposição genética é percebida pelo fato de que "apenas" 10% a 20% dos tabagistas desenvolvem DPOC. Além disso, há um maior risco de DPOC entre fumantes da mesma família e entre gêmeos. Outro dado que salienta o componente genético é que "apenas" 5% dos fumantes de etnia oriental desenvolvem a doença. No entanto, ainda não está bem estabelecido quais cromossomos seriam os responsáveis por tal predisposição. Uma causa de origem genética bem documentada para o surgimento da DPOC, embora rara, é a deficiência de alfa-1 antitripsina.
10 - Qual o papel da deficiência de alfa-1 antitripsina na DPOC?
A alfa-1 antitripsina (AAT) é uma glicoproteína constituída por uma cadeia de 394 aminoácidos e três cadeias laterais de carboidratos. A sua transmissão genética é do modo simples, autossômico, com dois alelos, sendo cada um de um dos progenitores, transmitindo aos filhos a expressão genética em 50%. A despeito de seu nome relacioná-la à inibição da tripsina, ela é capaz de inibir várias proteases séricas, constituindo excelente defesa do organismo contra agentes agressores. No entanto, a sua ação mais importante é a inibição da elastase produzida pelos neutrófilos, a qual tem a capacidade de digerir a elastina. A maior parte da alfa-1 antitripsina é produzida no fígado, sendo o restante derivado dos macrófagos e do epitélio brônquico.
A sua deficiência é uma condição rara (1% a 2% de toda a população com DPOC) e está associada ao desenvolvimento de enfisema, em pessoas jovens, com predomínio nas bases, o qual é classificado como panacinar. Estes pacientes habitualmente são subdiagnosticados e ficam rotulados como portadores apenas de doença pulmonar obstrutiva crônica (DPOC). Maiores detalhes sobre esta doença podem ser obtidos no simpósio “Abordagem atual do tratamento da deficiência de alfa-1 antitripsina”.
11 - Que outros fatores podem contribuir no surgimento ou progressão da DPOC?
Alguns fatores têm sido associados a maior risco de DPOC. São eles:
Idade: provavelmente o risco maior com a idade representa maior exposição ao longo da vida;
Sexo: a maior ocorrência no sexo masculino decorre apenas da maior prevalência do tabagismo.
Alguns estudos sugerem inclusive que mulheres são mais susceptíveis ao cigarro do que homens;
Fatores que comprometem o crescimento pulmonar na vida intra-uterina e na infância (tabagismo materno e domiciliar, infecções, desnutrição) favorecem a DPOC, na medida em que limitam a função pulmonar máxima alcançada, fazendo com que, com o declínio da mesma, os sintomas surjam mais precocemente;
Infecções: HIV, tuberculose e paracoccidioidomicose podem acelerar a piora da função pulmonar na DPOC;
Asma: alguns estudos sugerem a asma como fator de risco para DPOC, mesmo após ajustes para a carga tabagística.
12 - O que é limitação do fluxo aéreo e qual a sua causa?
A limitação ou obstrução do fluxo aéreo é a resistência à passagem de ar pelas vias aéreas, principalmente pelas de menor calibre. É a característica principal das doenças obstrutivas pulmonares, entre elas a DPOC. Esta limitação do fluxo aéreo, a partir de uma determinada intensidade, impede a expiração completa, gerando aprisionamento aéreo (hiperinsuflação). A limitação ao fluxo aéreo e o aprisionamento aéreo resultante são responsáveis pelo desenvolvimento do principal sintoma da DPOC que é a dispneia.
Uma mistura variável de doença das pequenas vias aéreas (bronquiolite obstrutiva) e destruição parenquimatosa (enfisema pulmonar) responde pela limitação ao fluxo aéreo na DPOC. Admite-se hoje que tais alterações sejam decorrentes de inflamação pulmonar, atingindo brônquios, bronquíolos e parênquima pulmonar, inflamação essa determinada principalmente pela inalação prolongada de substâncias nocivas. Associadamente a essas alterações existe hipertrofia das glândulas mucosas e das células caliciformes em vias aéreas centrais, responsáveis pela hipersecreção mucosa observada na DPOC. Frequentemente as alterações de hipersecreção precedem à limitação do fluxo, o que significa que tosse e expectoração geralmente precedem a dispneia.
13 - Quais são as consequências da hiperinsuflaçao na DPOC?
A hiperinsuflação decorre da obstrução ao fluxo aéreo, sobretudo quando há perda da sustentação das pequenas vias aéreas pelos alvéolos. Com ela, há aumento da capacidade residual funcional e redução da capacidade inspiratória, sobretudo durante a atividade física, quando a ventilação necessária para exercê-la aumenta (hiperinsuflação dinâmica). A hiperinsuflação ainda altera a conformação do diafragma e reduz sua capacidade contrátil. Todas essas alterações determinam dispneia, mais intensa aos esforços, e limita a capacidade de realizar atividades físicas.
14 - Quais são as mudanças patológicas encontradas na DPOC?
Mudanças patológicas características da DPOC são encontradas nas vias aéreas proximais, vias aéreas periféricas, parênquima pulmonar e vasculatura pulmonar. Essas mudanças incluem inflamação crônica e mudanças estruturais resultantes de lesões e reparos repetidos (tabela 2).
15 - Quais são os aspectos importantes na patogênese da DPOC?
A inflamação no trato respiratório de pacientes com DPOC parece ser uma amplificação da resposta inflamatória normal do trato respiratório a irritantes crônicos como fumaça de cigarro. Os mecanismos para essa ampliação ainda não são bem compreendidos, mas podem ser geneticamente determinados. Alguns pacientes desenvolvem DPOC sem fumar, mas a natureza da resposta inflamatória nesses pacientes é desconhecida. A inflamação pulmonar é adicionalmente amplificada pelo estresse oxidativo e o excesso de proteinases no pulmão. Juntos, esses mecanismos levam à mudanças patológicas características da DPOC.
16 - Qual o papel do estresse oxidativo e do desequilíbrio protease-antiprotease na gênese DPOC?
O estresse oxidativo pode ser um importante mecanismo amplificador na DPOC. Biomarcadores do estresse oxidativo (ex.: peróxido de hidrogênio, 8-isoprostano) estão aumentados no ar exalado e condensado, no muco e na circulação sistêmica dos pacientes com DPOC. O estresse oxidativo se eleva ainda mais nas exacerbações.
Os oxidantes são gerados por fumaça de cigarro e outros particulados inalados e liberados de células inflamatórias ativadas, como macrófagos e neutrófilos. Pode também haver uma redução nos antioxidantes endógenos em pacientes com DPOC. O estresse oxidativo tem várias consequências adversas nos pulmões, incluindo ativação de genes inflamatórios, inativação de antiproteases, estimulação de secreção do muco e estimulação do aumento da exsudação plasmática. O estresse oxidativo pode também ser responsável por uma redução da atividade das histona-deacetilases nos tecidos pulmonares dos pacientes com DPOC, que pode levar a uma expressão elevada de genes inflamatórios como também à redução na ação anti-inflamatória dos corticoides.
Existem evidências persuasivas para a existência de um desequilíbrio entre as proteases nos pulmões de pacientes com DPOC, que destroem os componentes do tecido conjuntivo, e as antiproteases, que protegem contra isso. Várias proteases derivadas das células inflamatórias e células epiteliais estão elevadas em pacientes com DPOC. Há um aumento nas evidências que elas podem interagir entre si, contribuindo para a destruição do parênquima pulmonar resultando no enfisema.
Capítulo 4 - Quadro Clínico
17 - Como é a apresentação clínica da DPOC?
O estereótipo do portador de DPOC é aquele indivíduo com idade superior a 40 anos e tabagista de longa data (fumou, em média, mais de um maço/dia por 20 anos ou equivalente), que apresenta sintomas respiratórios crônicos. Esses sintomas são:
Tosse e produção de escarro
Inicialmente o paciente apresenta tosse pela manhã, que pode ser produtiva ou não. Nesta fase inicial da doença, o paciente a rotula como um "pigarro" e tende a não lhe dar muita importância. Com a passagem dos anos, a tosse tende a tornar-se produtiva e constante, sendo que na maior parte do tempo o aspecto da secreção é mucoide. A mudança do aspecto de mucoide para purulento reflete o aumento da inflamação e deve levar à consideração de exacerbação de etiologia bacteriana.
Dispneia
Apresenta-se inicialmente aos grandes esforços, como subir escada ou ladeira ou andar depressa. Nesta fase, em função do sedentarismo, é comum o paciente atribuir a sua falta de ar “à idade”. A dispneia costuma ser progressiva e, com o passar dos anos, ela pode estar presente aos esforços das atividades da vida diária, como trocar de roupa, nas relações sexuais ou carregar uma sacola. É comum o paciente valorizar a dispneia somente nesta fase mais avançada, fato que contribui para o atraso do diagnóstico da enfermidade.
Sibilância
É relatada em intensidade variável, podendo estar ausente em alguns pacientes.
Outros
Sensação de aperto no peito: mal localizado, geralmente desencadeado por atividade física, tem caráter muscular. Acredita-se decorrer de contração isométrica dos músculos intercostais;
Fadiga;
Anorexia e emagrecimento: presentes nas doenças avançadas;
Sintomas de depressão e ansiedade: devem ser buscados ativamente.
18 - Como é a evolução dos sintomas da DPOC?
A DPOC é uma doença progressiva, no entanto a velocidade desta progressão varia de paciente para paciente e de acordo com as intervenções terapêuticas adotadas. A cessação do tabagismo é a medida mais importante para reduzir a progressão da DPOC.
No início da doença, todos os sintomas são leves e não constantes, podendo haver intensificação dos mesmos (exacerbações) em intervalos variáveis. Com o progredir da doença, os sintomas ficam mais intensos e frequentes e as exacerbações ocorrem mais amiúde. Nos estádios mais avançados a dispneia torna-se incapacitante, limitando significativamente a vida do paciente. Nesta fase pode surgir hipoxemia e, consequentemente, cor pulmonale (insuficiência ventricular direita secundária à hipertensão arterial pulmonar). Posteriormente os indivíduos podem evoluir com hipercapnia crônica.
19 - Quais são os achados do exame físico do paciente com DPOC?
O exame físico do paciente com DPOC pode variar de normal, ou quase normal, a acentuadamente alterado, dependendo da fase em que se encontra a doença. No paciente com DPOC em estádio inicial, são poucas as alterações observadas no seu exame. A inspeção, a palpação e a percussão são normais na grande maioria dos casos. Podem ser observados sibilos, principalmente à expiração forçada (é importante não se esquecer deste recurso propedêutico no exame de pacientes com doenças obstrutivas). A ausculta sem expiração forçada pode ser completamente normal. Roncos também podem estar presentes.
Aquele exame classicamente descrito de tórax em tonel, com redução do espaço da fúrcula esternal à cartilagem cricoide, com hipersonoridade à percussão e murmúrio vesicular diminuído à ausculta, só vai estar presente nos pacientes em fase avançada da doença. Importante destacar que o sinal mais específico para a detecção desta hiperinsuflação pulmonar é a medida da altura laríngea. Esta medida (espaço entre a fúrcula e a cartilagem cricóide) deve ser feita ao final da expiração, e valores menores que 4 cm indicam hiperinsuflação pulmonar.
Nas fases avançadas da DPOC podemos observar ainda sinais de cor pulmonale, ou seja, sinais de insuficiência cardíaca direita: turgência jugular, hepatomegalia e edema de membros inferiores.
20 - Quais as co-morbidades mais frequentes em pacientes com DPOC e que devem ser buscadas ativamente?
Pacientes com DPOC apresentam com frequência co-morbidades, em função da faixa etária em que a doença ocorre, do tabagismo como principal agente etiológico, do seu caráter crônico, do sedentarismo e das alterações nutricionais decorrentes das limitações da doença. As principais co-morbidades são:
doenças cardiovasculares;
doenças músculo-esqueléticas;
síndrome metabólica;
depressão;
osteoporose;
câncer de pulmão.
21 - Quais são os diagnósticos diferenciais mais importantes na DPOC?
A asma é um dos principais diagnósticos diferenciais da DPOC, sendo que, em alguns pacientes, ambas as doenças podem coexistir, não sendo possível diferenciá-las. Veja na tabela 3 os principais diagnósticos diferenciais e as características que auxiliam na sua distinção da DPOC.
22 - Como diferenciar DPOC de asma?
Às vezes é difícil fazer o diagnóstico diferencial entre asma e DPOC, principalmente naquele paciente na fase inicial da DPOC, ou seja, aquele paciente que ainda não tem uma história muito prolongada de sintomas respiratórios e que apresenta agudizações mais espaçadas, principalmente no período do inverno. Veja na tabela 4 as principais diferenças entre DPOC e asma.
A despeito disso, calcula-se que aproximadamente 20% dos pacientes com DPOC apresentem características asmáticas. Nessa situação o tratamento da DPOC será praticamente igual ao tratamento da asma. Por outro lado, algumas formas de asma comportam-se como DPOC, ou seja, mantêm quadro obstrutivo persistente a despeito do tratamento adequado. Tais quadros, principalmente quando se desenvolvem em indivíduos fumantes, não têm como ser diferenciados da DPOC. A despeito desta obstrução brônquica fixa, a asma não deve ser considerada como DPOC. O dado aqui indicativo de asma, na maioria das vezes, é a história de asma na infância.
A importância em se diferenciar essas duas entidades reside no fato de que a base do tratamento adequado da asma é o uso de corticoide inalado, enquanto que o tratamento da DPOC se fundamenta, até o momento, no uso de broncodilatadores, com os esteroides inalatórios reservados apenas para alguns pacientes.
Capítulo 5 - Exames Complementares
23 - Qual o principal exame complementar para o diagnóstico da DPOC?
A espirometria é o exame complementar que, em conjunto com um quadro clínico compatível, define o diagnóstico de DPOC ao mostrar um distúrbio ventilatório obstrutivo que não se normaliza após a administração de broncodilatador. A espirometria ainda auxilia na definição da gravidade da DPOC, que ajuda na escolha do tratamento a ser instituído.
24 - Qual a orientação do GOLD para a suspeita de DPOC e a realização de espirometria?
A DPOC deve ser lembrada e a espirometria solicitada em indivíduos com mais de 40 anos e que apresentam uma das seguintes características:
Dispneia progressiva, que caracteristicamente piora com o esforço, persistente;
Tosse crônica, que pode ser persistente ou intermitente, seca ou produtiva;
Produção crônica de escarro;
História de exposição a fatores de risco: tabagismo, exposição à queima de lenha, exposições ocupacionais (poeiras ou químicas);
História familiar de DPOC.
25 - A espirometria pode ser dispensável no diagnóstico de DPOC?
Não se justifica a ausência da espirometria em locais onde ela possa ser feita. No entanto, se tivermos um paciente com história típica de DPOC, com exame físico e radiografia de tórax compatíveis e que afastam a possibilidade de outras doenças, e se está em um local onde a espirometria não é possível de ser realizada, o tratamento para DPOC deverá ser iniciado.
26 - A medida do pico do fluxo expiratório é um bom método para seguir ou diagnosticar pacientes com DPOC?
O pico do fluxo expiratório (PFE ou “peak flow”) é usado algumas vezes como medida da limitação do fluxo aéreo, mas na DPOC ele pode subestimar o grau de obstrução das vias aéreas. Dados da US National Health and Nutrition Examination Survey sugerem que o pico do fluxo expiratório tem boa sensibilidade, identificando mais de 90% dos casos de DPOC diagnosticados pela espirometria. No entanto, porque sua especificidade é mais fraca, não deve ser utilizado como o único teste diagnóstico.
27 - Como interpretar a espirometria na DPOC?
O primeiro passo na interpretação da espirometria é observar a relação do volume expiratório forçado no primeiro segundo e a capacidade vital forçada, ou seja, a relação VEF1/CVF. Ela expressa a porcentagem de ar que o paciente consegue expirar no primeiro segundo, em relação ao total de volume de ar expirado. Uma pessoa normal expira no primeiro segundo, aproximadamente, 80% do volume total expirado. No entanto, o valor exato varia de acordo com a idade, altura e sexo do paciente, sendo que tais valores previstos podem ser encontrados em tabelas. Para simplificar a interpretação da relação VEF1/CVF na DPOC, os epidemiologistas concordaram em fixar este valor em 0,70, após o uso do broncodilatador. Assim, quando a relação for menor que 0,70, a pessoa está expirando menos do que deveria, caracterizando uma situação de limitação ao fluxo aéreo, também conhecida como obstrução das vias aéreas. Nesses casos, o passo seguinte consiste em avaliar o VEF1 isoladamente, para caracterizar o grau ou intensidade da limitação ou obstrução.
Em duas situações a relação VEF1/CVF pode estar abaixo de 0,70 e ser considerada normal: em pessoas muito altas, quando a CVF é muito elevada, ou em pessoas idosas, pois o VEF1 pode estar normalmente diminuído pela perda fisiológica da pressão de retração elástica pulmonar.
Se o diagnóstico for de distúrbio ventilatório do tipo obstrutivo, o terceiro passo é avaliar a CVF. Nas fases iniciais da DPOC ela é normal. No entanto, à medida que a DPOC progride e o paciente torna-se hiperinsuflado, o volume residual aumenta e comprime a CVF, diminuindo-a. Assim, quanto menor a CVF nos pacientes com DPOC, mais hiperinsuflado e mais grave ele deve estar.
De maneira resumida, as alterações espirométricas na DPOC podem ser apresentadas conforme ilustrado na tabela 5.
28 - O que é a prova broncodilatadora na espirometria?
É a determinação dos valores espirométricos após uso de broncodilatador inalado, geralmente um beta-dois adrenérgico, embora o teste possa também ser feito com um anticolinérgico. Um aumento do VEF1 e ou da CVF pós-broncodilatador em relação ao pré-broncodilatador igual ou superior a 12% e com valor absoluto desta variação igual ou superior a 200 ml caracteriza um teste positivo. Isto indica que existe um grau de reversibilidade importante do distúrbio funcional, sendo esta variação mais típica da asma, mas podendo ser também observada em pacientes com DPOC que apresentem broncoespasmo reversível associado. Caso o valor percentual pós-broncodilatador chegue a níveis de normalidade, a espirometria é fortemente sugestiva do diagnóstico de asma. A ausência de resposta broncodilatadora é típica da DPOC, mas não significa que o broncodilatador não será benéfico para o paciente.
29 - Qual a importância da radiografia de tórax no diagnóstico da DPOC e quando solicitá-la?
A radiografia torácica é importante no sentido de excluir outras condições que possam levar à confusão diagnóstica com a DPOC ou estarem associadas à mesma, principalmente câncer, tuberculose e bolhas pulmonares. Outra condição em que a radiografia é útil é no sentido de fazer o diagnóstico diferencial com insuficiência cardíaca e doença intersticial pulmonar, principalmente naqueles pacientes com crepitações basais. Nas agudizações graves a radiografia de tórax é importante para verificar a presença de pneumotórax ou consolidação pulmonar.
O diagnóstico da DPOC não se baseia normalmente em dados radiográficos, pois os achados típicos de hiperinsuflação só ocorrem em doença avançada. A frequente descrição de sinais de hiperinsulflação em laudos radiológicos, na maioria das vezes, reflete apenas uma radiografia feita em inspiração profunda em paciente com tórax mais alongado.
A maioria dos pacientes com DPOC, principalmente nas fases iniciais da doença, apresenta radiografia de tórax normal, ou quase normal. Lembre-se que uma radiografia com sinais importantes e definidos de hiperinsulflaçâo deve sempre se associar à observação de importantes alterações ao exame físico.
De maneira prática, a radiografia de tórax deve ser solicitada quando da primeira avaliação do paciente com suspeita de DPOC. Nos indivíduos que já têm o diagnostico da doença, a radiografia torácica deverá ser solicitada nas exacerbações em que não está havendo resposta ao tratamento habitual e nas com indicação de internação. Não existe um intervalo de tempo definido para se repetir a radiografia de tórax de paciente com DPOC após a primeira avaliação, sendo discutível a repetição anual deste exame.
30 - Existe indicação de solicitação de tomografia computadorizado de tórax na rotina?
Não. A tomografia computadorizada de tórax só deve ser solicitada quando há dúvida quanto ao diagnóstico (ex. suspeita de doença intersticial), na suspeita de outras doenças associadas (ex. bronquiectasias, tumor) ou quando se planeja a realização de cirurgia redutora de volume pulmonar (para avaliar a distribuição das áreas de enfisema, fator determinante na indicação da cirurgia).
31 - Quando deve ser realizada oximetria de pulso e quando deve ser solicitada a gasometria arterial no paciente com DPOC?
A oximetria deve ser realizada em pacientes estáveis e com VEF1
32 - Que outras avaliações podem ser feitas na DPOC?
Outras avaliações funcionais não realizadas rotineiramente podem ser indicadas em condições específicas:
Medidas dos volumes pulmonares por pletismografia ou diluição com Hélio: avalia a hiperinsuflação;
Difusão de monóxido de carbono (DLCO): avalia o impacto funcional do enfisema, estando indicada em pacientes com dispneia desproporcional ao nível de obstrução ao fluxo aéreo;
Testes de exercício: têm valor prognóstico e alguns podem auxiliar na prescrição da atividade física nos programas de reabilitação, além de poderem documentar melhoras obtidas com os mesmos:
Teste de caminhada de 6 minutos;
Shuttle;
Teste cardio-pulmonar;
33 - Quando investigar a deficiência de alfa-1 antitripsina nos pacientes com DPOC?
As principais indicações de pesquisa de deficiência de alfa-1 antitripsina, segundo a American Thoracic Society e a European Respiratory Society (2002), são:
Enfisema de início precoce (menos de 45 anos);
Enfisema na ausência de exposição a fatores de risco conhecidos (tabagismo, fatores ocupacionais);
Enfisema predominantemente basal;
Caso de deficiência de alfa-1 antitripsina confirmado na família;
História familiar de enfisema, bronquiectasias, doença hepática ou paniculite;
Todos os indivíduos com doença pulmonar obstrutiva crônica;
Pacientes com asma cuja espirometria não normaliza apesar de tratamento adequado;
Adultos com bronquiectasias sem causa definida;
Doença hepática sem causa definida;
Paniculite necrosante;
Vasculite relacionada ao anticorpo anticitoplasma de neutrófilo;
Confirmação de ausência de banda alfa-1 em eletroforese de proteínas séricas.
Capítulo 6 - Classificação
34 - Que parâmetros devem ser utilizados no estadiamento da DPOC?
Os parâmetros utilizados para caracterizar a gravidade da DPOC devem ser aqueles que avaliam a intensidade dos sintomas atuais e os riscos de agravamento da doença, sobretudo o risco de ocorrência de exacerbações, que sabidamente impactam negativamente a evolução da DPOC. Os parâmetros atualmente recomendados são:
Escala de dispneia do Medical Research Council Modificada;
Questionário para avaliação da DPOC (CAT – COPD assessment test);
Espirometria: apesar de não haver uma boa correlação com sintomas e qualidade de vida, a espirometria correlaciona-se com o risco de exacerbações;
Número de exacerbações por ano: o principal preditor de ocorrência de exacerbação no futuro é a história de exacerbações prévias.
35 - Como a escala de dispneia do Medical Research Council (MRC) foi modificada para emprego na DPOC?
O MRC modificado para avaliação da dispneia a DPOC varia de 0 a 4:
Grau 0: apresenta-se com dispneia somente com exercícios extenuantes;
Grau 1: apresenta-se com dispneia quando anda mais rapidamente no plano ou quando anda em pequeno aclive;
Grau 2: anda mais devagar em comparação com pessoa da mesma idade em função de dispneia, ou tem que parar para respirar quando ando no próprio passo e no plano;
Grau 3: para para respirar após andar 100 metros ou poucos minutos, no plano;
Grau 4: muito dispneia para sair de casa, sente dispneia ao vestir-se ou despir-se.
36 - O que é questionário CAT e como ele é aplicado?
Trata-se de um teste auto-aplicável com 8 itens para avaliação da DPOC, sendo validado para diferentes línguas, incluindo o português. Cada item pode ser pontuado entre 0 a 5, gerando um escore que varia de 0 a 40, sendo que quanto maior o escore, pior o estado de saúde relacionado à DPOC (tabela 6).
O questionário está disponível em: http://catestonline.org
37 - Qual a classificação da gravidade da obstrução na DPOC pela espirometria?
Com base na espirometria, a DPOC é classificada em:
Leve (GOLD 1): VEF1 > 80%;
Moderada (GOLD 2): 50%
Grave (GOLD 3): 30%
Muito grave (GOLD 4): VEF1
38 - Como se classificação a gravidade da DPOC com base nos parâmetros apresentados, segundo o GOLD (2015)?
O documento GOLD sugere classificar a DPOC com base nos sintomas atuais, estimados pela escala de dispneia MRC e pelo CAT, e nos riscos futuros, estimados pela DPOC ou pelo número de exacerbações no ano anterior. Figura 1.
39 - O que é o escore BODE?
O escore BODE foi criado para englobar quatro aspectos importantes na DPOC: massa corpórea (B de body mass index), obstrução das vias aéreas (O de obstruction), dispneia (D de dyspnea) e capacidade de exercício (E de exercise). Ele inclui, portanto, dois descritores de envolvimento sistêmico da DPOC, o índice de massa corpórea e a distância caminhada em seis minutos; um que envolve o sintoma mais importante de que se queixa o paciente com DPOC, a dispnéia (avaliada pelo MRC); e um fator que avalia o pulmão, o órgão diretamente afetado pela doença, o VEF1. Embora os estudos clínicos envolvendo esse novo escore tenham mostrado que ele é superior ao VEF1 isoladamente como preditor de mortalidade na DPOC, talvez por sua relativa complexidade, o BODE não tem sido aplicado no dia a dia.
Quanto maior a pontuação, pior o prognóstico.
Capítulo 7 - Tratamento
40 - O que é DPOC estável?
É a fase da DPOC em que o paciente apresenta estabilidade clínica dos sintomas tosse, produção de escarro e falta de ar. Nessa fase pode haver pacientes que ficam praticamente assintomáticos e não têm indicação para uso de qualquer medicação, mas há os que apresentam sintomas persistentes e que necessitam de uso regular de medicação sintomática, de acordo com o seu estadiamento.
41 - Quais são os objetivos do tratamento da DPOC?
Embora a DPOC seja uma doença não completamente reversível, existem tratamentos comprovadamente eficazes e que devem empregados com os seguintes objetivos:
Reduzir sintomas
Reduzir os sintomas da doença;
Aumentar a tolerância ao exercício;
Melhorar a qualidade de vida;
Reduzir os riscos da doença
Prevenir a progressão da doença;
Prevenir e tratar as exacerbações;
Reduzir a mortalidade;
Reduzir eventos adversos associados ao tratamento.
Diagnóstico resolvido por componentes: quando deveria ser utilizado?
Component resolved diagnosis: when should it be used? (Diagnóstico resolvido por componentes: quando deveria ser utilizado?) Luengo O, Cardona V. Clin Transl Allergy. 2014 Sep 8;4:28. doi: 10.1186/2045-7022-4-28. eCollection 2014.
Abstract:
The knowledge on molecular allergy diagnosis is continuously evolving. It is now time for the clinician to integrate this knowledge and use it when needed to improve the accuracy of diagnosis and thus provide more precise therapeutic and avoidance measures. This review does not intend to comprehensively analyze all the available allergen molecules, but to provide some practical clues on use and interpretation of molecular allergy diagnosis. The potential role of component resolved diagnosis in circumstances such as the indication of allergen immunotherapy, pollen polysensitization, food allergy, latex allergy or anaphylaxis, is assessed. Interpreting the information provided by molecular allergy diagnosis needs a structured approach. It is necessary to evaluate single positivities and negativities, but also to appraise "the big picture" with perspective.
Comentários DE DR. ATAUALPA REIS:
O conhecimento do diagnóstico molecular da alergia está aumentando continuamente. É necessário que o clínico integre este conhecimento e o utilize quando necessário para melhorar a acurácia do diagnóstico e fornecer medidas terapêuticas e de exclusão mais precisas. Esta revisão não analisa completamente todos os alérgenos moleculares, mas fornece algumas dicas práticas sobre a utilização e interpretação do diagnóstico molecular da alergia.
O diagnóstico por componentes pode ser utilizado na indicação da imunoterapia alérgica, sensibilização múltipla (pólen e alimentos), alergia alimentar (avaliação de risco e de co-fatores), alergia a látex ou anafilaxia.
Anafilaxia
Dados epidemiológicos demonstram que os co-fatores (exercícios, álcool, antiinflamatórios, etc) são relevantes em até 39% dos casos de anafilaxia por alimentos em adultos. A alergia a trigo induzida por exercício é a que melhor caracteriza estes casos e está classicamente relacionada à sensibilização à ômega-5 gliadina. As proteínas transportadoras de lípedes não específicas (nsLTP) também são consideradas importantes co-fatores para alergia alimentar, principalmente relacionada aos vegetais, oleaginosas e cereais, na população mediterrânea. Pacientes com história de reação anafilática relacionada à co-fatores podem ser investigados quanto à presença de imunoglobulina E sérica (sIgE) para nsLTP (especialmente Pru p 3, mas também Tri a 14) e para ômega-5 gliadina.
Em pacientes com história de reação anafilática tardia (3-6 horas após ingestão) para carnes de mamíferos, a sIgE para galactose-alfa-1,3-galactose (alfa-gal) deve ser investigada. Tem sido sugerido que picadas de carrapato sejam os responsáveis por desenvolvimento de sIgE para alfa-gal.
O diagnóstico por componentes múltiplos e a sIgE podem ser utilizados para casos de anafilaxia idiopática.
Alergia ao látex
O diagnóstico por componentes permite diferenciar os pacientes apenas sensibilizados ao látex e aqueles com verdadeira alergia ao látex. Pacientes sensibilizados apenas ao Hev b 8 são assintomáticos à exposição ao látex.
Sensibilização aos múltiplos alérgenos alimentares
Reações alérgicas a frutas e vegetais pode ser resultado de uma sensibilização primária a alimentos ou a inalantes. Em geral, a reatividade cruzada é atribuída à alérgenos lábeis (por exemplo, PR-10 ou profilinas) e associada com reações orais leves, enquanto que os alérgenos resistentes ao calor e à proteólise, estão geralmente associados com reações sistêmicas além das reações locais e com sensibilização primária pela via oral (por exemplo, proteína de estoque e nsLTP).
Avaliação de risco na alergia alimentar
A avaliação por componentes permite detectar os pacientes com maior risco de reações graves. Os principais componentes são aqueles relacionados à nsLTP e proteínas de estocagem.
Interpretar a informação fornecida pelo diagnóstico molecular necessita de uma abordagem estruturada. É necessário avaliar pontos positivos e negativos, mas também avaliar o cenário como um todo em perspectiva.
Determinação de IgE a alérgenos alimentares por microarray
(ImmunoCAP-ISAC) em pacientes com rinite alérgica Agosto 2013 - Volume 1 - Número 4
Evaluation of IgE antibodies to food allergens in patients with allergic rhinitis using microarray analysis (ImmunoCAP ISAC)
Laura Maria Lacerda Araujo1; Nelson Augusto Rosário Filho2
.
RESUMO
OBJETIVO: Determinar a frequência de anticorpos IgE a alérgenos alimentares em pacientes com doenças alérgicas respiratórias por análise molecular.
MÉTODO: Este estudo transversal incluiu 101 participantes, com idades entre 6-18 anos, com diagnóstico de rinite alérgica (89,1% com asma associada), sem história de alergia alimentar. Foi realizada análise de IgE sérica específica por ImmunoCAP ISAC, método que emprega biologia molecular para detecção de IgE a componentes alergênicos, sendo 42 alimentares e provenientes das seguintes fontes: abacaxi, aipo, amendoim, avelã, bacalhau, camarão, carpa, castanha de caju, castanha do Pará, cenoura, gergelim, kiwi, leite de vaca, maçã, ovo, pêssego, soja e trigo. Valores > 0,3 ISU (unidades padronizadas do ISAC) foram considerados positivos. Utilizou-se análise estatística descritiva.
RESULTADOS: Vinte e sete (26,7%) pacientes apresentaram IgE específica a pelo menos um dos alérgenos alimentares analisados. Entre os 42 componentes alergênicos testados, 20 (47,6%) foram associados a resposta IgE em pelo menos um dos pacientes. Alérgenos com maior frequência de reatividade IgE foram: camarão (Pen a 1 15,8%, Pen i 1 16,8%, Pen m 1 16,8%) e pêssego (Pru p 3 5,9%).
CONCLUSÕES: Este estudo demonstrou que a avaliação de alergia alimentar baseada em análise molecular deve considerar vários elementos, particularmente a correlação com os sintomas clínicos, e o conhecimento sobre reatividade cruzada IgE entre alérgenos das mais variadas fontes. Presença de IgE específica a determinado componente alergênico significa sensibilização, e não necessariamente alergia. Diagnóstico incorreto de alergia alimentar pode levar a tratamento inadequado, com dietas restritivas desnecessárias e prejuízo nutricional para os pacientes.
Palavras-chave: Sensibilização, alérgenos alimentares, alergia respiratória, IgE.
INTRODUÇÃO
O diagnóstico baseado na alergia molecular (diagnóstico molecular, DM) é utilizado para mapear a sensibilização alérgica de um paciente em nível molecular, por meio de componentes alergênicos em substituição a extratos alergênicos totais. Desde a sua introdução, no final da década de 1980, quando tecnologia de DNA foi aplicada para clonar e caracterizar moléculas alergênicas, DM vem sendo empregado na prática clínica do alergista1,2. Atualmente, mais de 130 componentes alergênicos estão comercialmente disponíveis para utilização em ensaios para dosagens de IgE específica sérica.
Um dos principais papeis da alergia molecular é no diagnóstico e prevenção da alergia alimentar. O conhecimento de componentes alergênicos aos quais o paciente é sensibilizado pode ajudar a diferenciar se há uma predisposição a reações locais ou sistêmicas e à persistência de sintomas clínicos. Outro aspecto relevante, difícil de ser definido por meio dos métodos tradicionais de detecção de IgE específica (in vivo ou in vitro), é a identificação de resposta IgE a alérgenos que apresentam estabilidade. Alérgenos que são estáveis ao calor ou à digestão geralmente provocam reações clínicas mais graves, enquanto os componentes alergênicos lábeis, em sua maioria provocam sintomas mais leves2. O DM pode ainda diferenciar se há sensibilização genuína a um alérgeno ou se ela ocorre por reatividade cruzada entre componentes alergênicos, ajudando a identificar predisposição a reação após exposição a diferentes fontes alergênicas2,3.
O objetivo deste estudo foi verificar a frequência de resposta IgE a alérgenos alimentares por meio de análise molecular em pacientes com doenças alérgicas respiratórias.

Diagnóstico de alergia entra na era molecular
Publicado em: 19/03/2013 Por:Fleury Medicina e Saúde
Teste baseado em microarray permite a detecção simultânea da IgE específica de mais de 110 componentes moleculares alergênicos.
Os métodos moleculares chegaram, enfim, à seara do diagnóstico de alergia. Acompanhando essa evolução, o Fleury acaba de introduzir, em sua rotina, o ImmunoCAP®Isac, que consiste em um imunoensaio de fase sólida, baseado em microarray, para a detecção e a determinação semiquantitativa da IgE específica de 112 componentes moleculares alergênicos, naturais ou recombinantes, de 51 diferentes origens, entre os relevantes, os tradicionalmente envolvidos em reações cruzadas e até os raros, potencialmente anafiláticos.
Dessa forma, o teste acelera o diagnóstico por analisar simultaneamente vários parâmetros, fornece o painel de sensibilização de IgE dos pacientes, acusa a presença de sensibilização para alérgenos de reatividade cruzada e permite a adoção de medidas profiláticas nesses casos, além de otimizar o esclarecimento de situações particulares, como a alergia alimentar e a alergia ao látex.
Apesar de se tratar de um método automatizado e de fácil execução, o ImmunoCAP®Isac só deve servir como screening em populações sintomáticas e nas quais a história clínica e os recursos tradicionais, como o teste cutâneo e a pesquisa de IgE específica para determinados alérgenos – conhecida como ImmunoCAP®, o método que substituiu o Rast – , não tenham sido suficientes para o diagnóstico.
Assim, o novo exame está particularmente indicado para confirmar as já mencionadas múltiplas sensibilizações, bem como para elucidar casos complexos de dermatite atópica, anafilaxia idiopática e ausência de resposta a tratamento, complementando, portanto, o arsenal-padrão nesse tipo de investigação.
O que é microarray?
A tecnologia de microarranjos de proteínas corresponde a pequenas placas de vidro ou de materiais sintéticos que recebem dezenas de microperfurações, com 100-200 μm de diâmetro, nas quais se aplicam diferentes tipos de tratamentos químicos para que haja a ligação covalente de proteínas. É aí que entram os componentes moleculares alergênicos.
Passo a passo do ImmunoCAP®Isac

1) Os componentes moleculares alergênicos ficam imobilizados no interior de cada micro-orifício do equipamento e são incubados com soro para a identificação de anticorpos IgE.
2) A localização de cada micro-orifício e de sua respectiva proteína é identificada por um conjunto de coordenadas (x e y).
3) Sobre a placa de microarranjos, aplica-se o soro do paciente, que cobre toda a superfície microperfurada, de modo que os anticorpos IgE existentes no material, específicos para cada alérgeno, acoplem-se às proteínas imobilizadas.
4) A adição de um anticorpo anti-IgE, com marcação fluorescente ou medidas de absorbância de radiação visível, possibilita a detecção da ligação entre os anticorpos e os alérgenos, à medida que ocasiona um sinal proporcional à quantidade de IgE originalmente ligada.
5) Um leitor de biochips fornece uma imagem que, analisada por um software de acordo com a intensidade da fluorescência, emite um padrão qualitativo que permite a identificação simultânea de diferentes IgEs específicas.

6) O equipamento compara as medidas de absorbância de cada IgE específica detectada com padrões internos, utilizados nos microarranjos, e as converte em medidas semiquantitativas.
7) Os valores são expressos em Isac Standardized Units (ISU), com cut-off de positividade de 0,3 ISU. Uma vez que as calibrações dos sistemas Isac e ImmunoCAP® (antigo Rast) diferem entre si, os resultados obtidos com as duas metodologias podem não ser quantitativamente comparáveis (abaixo).

Um olho no alérgeno alimentar e outro na reatividade cruzada
Além da sensibilização pela via gastrointestinal, que caracteriza os quadros de alergia alimentar, muitos casos também se devem à reatividade cruzada entre alérgenos alimentares e aeroalérgenos, a qual ocorre devido à homologia entre sequências de aminoácidos, à própria estrutura das proteínas, à existência de pan-alérgenos e até mesmo à ampla distribuição de proteínas alergênicas no reino vegetal, entre outros fatores. O conhecimento da reação cruzada em tais situações tem relevância tanto no diagnóstico quanto no tratamento, a fim de evitar restrições dietéticas desnecessárias. O mesmo vale para os determinantes de carboidratos de reação cruzada, ou CCD, do inglês cross-reactive carbohydrate determinants, que se encontram na maioria das plantas e podem levar à presença de IgE, mas são flagrados e devidamente eliminados pelo novo teste

Diagnóstico de alergia na era dos testes moleculares
Publicado em: 22/03/2013 Por
Dra. Barbara Gonçalves da Silva e Dra. Fernanda Aimée
Conceito de reação adversa a alimentos
O termo reação adversa a alimentos é utilizado para definir qualquer reação ocorrida após a ingestão de alimentos ou aditivos alimentares. Pode englobar desde a intolerância até a hipersensibilidade, ou alergia alimentar (Sampson, 2003).
A intolerância refere-se a qualquer resposta fisiológica a um alimento ou aditivo e é classificada em quatro tipos principais: toxicidade ou envenenamento, reação farmacológica, como a cefaleia que ocorre pela cafeína ou tiramina, resposta metabólica, como a diarreia em indivíduos com deficiência de lactase, e reações idiossincrásicas (Sampson, 2003).
Já a hipersensibilidade, ou alergia alimentar, diz respeito a reações a alimentos ou aditivos desencadeadas por mecanismos imunológicos, mediados ou não pela IgE. Apresenta um grande espectro de manifestações clínicas, desde quadros leves, com sintomas locais, como a síndrome da alergia oral e urticária de contato, até quadros sistêmicos e fatais, como a anafilaxia.
Dois padrões principais de sensibilização podem estar envolvdos na alergia alimentar: o que ocorre por meio da ingestão do alérgeno, via gastrointestinal, e o que se manifesta secundariamente a alérgenos inalantes, tendo por base um mecanismo imunológico de reatividade cruzada IgE-mediada, em que proteínas inaladas levam à produção de anticorpos da classe IgE com capacidade de reagir a proteínas de alimentos.
Diante da reatividade cruzada
O crescimento da prevalência de sensibilização aos aeroalérgenos tem-se refletido não só no aumento das manifestações alérgicas respiratórias, mas também no dos fenômenos de reatividade cruzada com alérgenos alimentares. São vários os determinantes da relevância clínica da reatividade cruzada: a característica da proteína alergênica, como homologia, solubilidade e estabilidade; fatores associados à exposição ao alérgeno; as proteínas alergênicas amplamente distribuídas na natureza (pan-alérgenos); e a concentração e a afinidade da IgE produzida, entre outros. Da mesma forma, a presença dos determinantes de carboidratos de reação cruzada (cross-reactive carbohydrate determinants, ou CCD) também é importante. Encontrados na maioria das plantas, os CCDs podem levar à produção de IgE, sendo rara a associação com sintomas clínicos (Schmid-Grendelmeier, 2010).
O fenômeno da reatividade cruzada, na alergia alimentar, tem implicações relevantes em termos de diagnóstico e tratamento. Assim, diante de um paciente com esse quadro, é fundamental a identificação do alérgeno suspeito e sua exclusão, bem como a prevenção de reações alérgicas causadas pela ingestão de alimentos com reatividade cruzada, de modo a evitar restrições dietéticas desnecessárias.
A maioria dos extratos usados na prática clínica para avaliação diagnóstica, tanto in vivo (testes cutâneos) como in vitro (IgE específica), corresponde a extratos proteicos complexos, obtidos a partir de fontes alergênicas naturais, o que leva à variabilidade em sua composição e alergenicidade. Dessa maneira, obtém-se informação relativa à fonte alergênica potencial, mas não se identifica a molécula que desencadeia os sintomas, o que só é possível com alérgenos naturais purificados ou alérgenos recombinantes.
Tecnologia molecular no diagnóstico de alergia
Visando a um correto diagnóstico do alérgeno alimentar envolvido e a uma redução das chances de obter resultados falso-positivos e falso-negativos nos exames laboratoriais, especialmente em indivíduos polissensibilizados, tem havido uma preocupação crescente em relação à melhoria dos métodos diagnósticos disponíveis, sobretudo os feitos in vitro.
Nesse sentido, a tecnologia molecular vem permitindo a clonagem e a produção de alérgenos das principais fontes alergênicas, em formas recombinantes, os quais mantêm as propriedades imunológicas das proteínas naturais, com consequente aumento da sensibilidade diagnóstica. Surge, então, o conceito de component-resolved diagnosis (CRD), ou seja, da identificação da molécula ou componente específicos do alérgeno envolvido na sensibilização, o que se tornou recentemente possível graças à tecnologia por biochip e ao desenvolvimento de testes de alergia miniaturizados (microarray).
Os testes de IgE baseados em microarray possibilitam acelerar o diagnóstico, devido à análise simultânea de vários parâmetros; determinar o componente molecular envolvido na sensibilização, e não somente a fonte alergênica; otimizar o diagnóstico de situações particulares, como a alergia alimentar e a alergia ao látex; utilizar uma amostra mínima de soro do doente (20-50 μL/teste); e ainda adotar medidas profiláticas, quando aplicáveis, em situações de reatividade cruzada; entre outros benefícios.
Imunoensaio com componentes moleculares alergênicos
O ImmunoCAP®Isac (Immuno Solid Phase Allergen Chip) é um teste in vitro que visa a identificar e determinar semiquantitativamente a presença de anticorpos específicos da classe IgE (sIgE) no soro ou no plasma humano para 112 componentes alergênicos, de 51 fontes, simultaneamente (Carvalho et al, 2010).
O exame consiste em um imunoensaio, em que os componentes alergênicos ficam imobilizados em um substrato sólido, na forma de microarray, e são incubados com 20 μL de soro do paciente para a detecção de anticorpos sIgE. A ligação entre esses anticorpos e os componentes alergênicos é identificada pela adição de um anticorpo anti-IgE, com marcação fluorescente. Com a utilização de um leitor de biochips, consegue-se uma imagem que, por meio da intensidade de fluorescência (valores FI), permite obter o resultado dos testes com a ajuda de um software adequado, o Microarray Image Analysis Software, de acordo com a metodologia do fabricante. Os resultados são expressos em Isac Standardized Units (ISU), com cut-off de positividade de 0,3 ISU (Carvalho et al, 2010). A partir dessa análise, é possível conhecer o painel de sensibilização de IgE do paciente para inúmeros componentes alergênicos e também observar a presença ou não de sensibilização para alérgenos de reatividade cruzada (Santos et al, 2010).
A validade desse teste múltiplo como screening depende de sua indicação adequada. Numa população sintomática, um resultado positivo aumenta a probabilidade de o paciente ser alérgico. Entretanto, quando o multiplex é utilizado em indivíduos não selecionados, pode haver resultados falso-negativos e falso-positivos. Desse modo, não é recomendável que o exame seja utilizado como “triagem”, sem uma indicação clínica específica (Bernstein et al, 2008).
Quando bem indicado, o ImmunoCAP®Isac tem muitas vantagens, tais como simplicidade, necessidade de mínimo volume de sangue e utilização de grande parte dos alérgenos relevantes, com capacidade de identificar CRDs, alérgenos de reação cruzada e alérgenos raros, potencialmente anafiláticos, além de eliminação dos CCDs (Ferrer et al, 2009; Schmid-Grendelmeier, 2010). Contudo, sua principal desvantagem ainda é o custo.
Na prática, o novo exame é recomendado especialmente em casos de suspeita de múltiplas sensibilizações e/ou possibilidade de sintomas desencadeados por reações cruzadas entre alérgenos, dermatite atópica, anafilaxia idiopática e ausência de resposta à exclusão de um alimento sabidamente implicado na alergia do paciente. No entanto, não substitui a história clínica, o teste cutâneo, a dosagem de IgE específica para um componente/painel ou a provocação oral, mas complementa a investigação do paciente (Schmid-Grendelmeier, 2010). Por outro lado, não há indicação na realização desse teste em indivíduos monossensibilizados.
Referências
Sampson, HA – Food Allergy. J Allergy Clin Immunol, 111: s540-547, 2003.
Schmid-Grendelmeier P – Recombinant allergens. Routine diagnostics or still only science? Der Hautartzt 2010, 61 (11): 946-953.
Carvalho S, Gaspar A, Prates S, Pires G, Silva I, Matos V, Loureiro V, Leiria-Pinto P - ImmunoCAP ISAC®: Tecnologia microarray no estudo da alergia alimentar em contexto de reactividade cruzada. Rev Port Imunoalergologia 2010; 18 (4): 331-352.
Santos KS; Kokron CM; Palma MS – Diagnóstico in vitro. Em: Diagnóstico. Castro FFM et al – Alergia Alimentar. Cap. 6, 53 – 74, Ed. Manole, 2010.
Bernstein Il et al – Allergy Diagnostic Testing: an updated practice parameter. Ann Allergy Asthma Immunol 2008, 100: S1 – 148.
Ferrer M; Sanz ML; Sastre J; et al – Molecular diagnosis in Allergology: application of the microarray tecnique. J Investig Allergol Clin Immunol 2009, 19 (1): 19-24
A alergia como nunca a viu
Thermo Fisher Scientific Inc. (NYSE: TMO)
Inclua os componentes dos alergénios no trabalho de diagnóstico e leve o diagnóstico de alergias a um novo nível. A alergologia molecular mede a sensibilização aos componentes individuais dos alergénios, o que oferece um quadro detalhado do perfil de sIgE do doente. Desta forma é possível avaliar o risco da alergia e explicar sintomas devidos à reactividade cruzada, ajudando-o a melhorar a gestão do doente.
A nova abordagem da Alergologia Molecular leva o diagnóstico mais longe através da quantificação dos anticorpos IgE específicos em moléculas de um alergénio único e puro. A precisão melhorada assim obtida reforça a utilidade clínica dos testes IgE.
Componentes de alergénios – a base de um diagnóstico melhorado
É possível produzir componentes alergénicos individuais a partir de uma fonte alergénica. Deste modo, a sensibilização a estes componentes é medida individualmente em testes separados, ajudando a identificar, com um nível molecular exacto, o componente ao qual o doente é sensível.
Esta informação fornece a base para um diagnóstico preciso da alergia. Na Alergologia Molecular, os testes com base em extractos são utilizados em conjunto com análises específicas de componentes. O extracto fornece a resposta global se o doente for sensível à fonte do alergénio em particular, enquanto os componentes oferecem informações adicionais sobre o risco, especificidade e reactividade cruzada.
O que nos podem dizer os componentes de alergénios?
Os componentes de alergénios são proteínas e, com base na semelhança estrutural, são agrupadas em diferentes famílias de proteínas. Dependendo das propriedades destas proteínas, a sensibilização aos componentes leva a diferentes consequências para o doente.

Componentes específicos: pistas únicas para revelar as fontes da alergia
Cada fonte de alergénio contém caracteristicamente componentes alergénios específicos e de reactividade cruzada. Os componentes específicos de alergénios são mais ou menos exclusivos da fonte, encontrados apenas num número limitado de espécies relacionadas. Cada fonte de alergénios pode conter um ou alguns componentes específicos de alergénios. A sensibilização a qualquer um deles indica uma sensibilização genuína, o que significa que a fonte de alergénios correspondente é a causa principal dos sintomas clínicos.
Identificar componentes de reactividade cruzada - melhorar o diagnóstico
Os componentes de alergénios de reactividade cruzada estão mais distribuídos e podem ser partilhados por uma vasta gama de fontes de alergénios. Devido à grande semelhança estrutural, podem provocar reactividade cruzada com anticorpos IgE.
A reactividade cruzada pode ser exemplificada com a alergia alimentar relacionada com o pólen de bétula, uma síndrome que afecta muitos doentes alérgicos ao pólen de bétula. O motivo molecular subjacente a esta reactividade cruzada é o facto de a maior parte dos doentes alérgicos ao pólen de bétula terem anticorpos IgE específicos do componente Bet v 1. Bet v 1 tem uma semelhança estrutural a proteínas relacionadas de vários alimentos, por exemplo a soja e o amendoim. Assim, os anticorpos IgE do doente para o Bet v 1 de bétula têm uma reacção cruzada com estas proteínas relacionadas da soja ou do amendoim.
Quantidade e estabilidade da proteína
Os componentes alergénicos dos alimentos apresentam diferentes estabilidades ao calor e à digestão, e o respectivo conteúdo na fonte de alergénios varia. Tanto a estabilidade como a quantidade são reflectidas pela família de proteínas a que pertence o componente. Assim, conhecendo o perfil de sensibilização do doente e a que família pertencem os componentes identificados, é possível avaliar o risco associado às sensibilizações.

42 - Qual a importância da cessação do tabagismo no tratamento do paciente com DPOC?
A cessação do tabagismo é a intervenção com maior capacidade de alterar a história natural da DPOC e por isso deve ser buscada em todos os pacientes, independentemente do estágio da doença em que se encontram. Maiores detalhes sobre os diferentes tratamentos do tabagismo estão em seu capítulo específico.
43 - Qual o arsenal farmacológico disponível para o tratamento da DPOC estável?
Existem diferentes classes de medicamentos para o tratamento da DPOC, com destaque para os broncodilatadores, indicados de alguma forma para todos os pacientes. A seguir listamos os medicamentos com o potencial de uso no tratamento da DPOC, embora em alguns casos com indicações muito restritas ou até mesmo discutíveis.
Broncodilatadores
Beta-2 agonistas
Curta ação (4-6 horas): salbutamol, fenoterol, terbutalino;
Longa ação
12 horas: formoterol e salmeterol;
24 horas: indacaterol, olodaterol e vilanterol (disponível apenas em associação com fluticasona).
Anticolinérgicos
Curta ação (6 horas): ipratrópio;
Longa ação: (24 horas): tiotrópio.
Xantinas
Aminofilina;
Teofilina;
Bamifilina.
Corticoides
Inalatórios: beclometasona, budesonida, fluticasona, mometasona;
Orais: prednisona, prednisolona, deflazacort.
Inibidores da fosfodiesterase 4:Roflumilast.
Mucolíticos e antioxidantes:
N-acetilcisteína;
Carbocisteína.
Alfa-1 antitripsina
44 - Como escolher dentre tantas opções de medicamentos para o tratamento da DPOC estável?
Em sua última revisão, o GOLD (2015) orienta o tratamento farmacológico com base na classificação da doença em A, B, C ou D, de acordo com a intensidade dos sintomas e com o risco de exacerbações.
A – Pacientes pouco sintomáticos e com baixo risco de exacerbação
1ª escolha: sem ordem de preferência
Anticolinérgico de curta ação sn ou
Beta-2 agonista de curta ação sn.
2ª escolha: sem ordem de preferência
Anticolinérgico de longa ação ou
Beta-2 agonista de curta ação ou
Associação de anticolinérgico de curta ação com beta-2 agonista de curta ação.
Alternativa: pode ser usada isoladamente ou em associação com as medicações descritas anteriormente
Teofilina.
B – Pacientes muito sintomáticos e com baixo risco de exacerbação
1ª escolha: sem ordem de preferência
Anticolinérgico de longa ação ou
Beta-2 agonista de longa ação.
2ª escolha
Associação de anticolinérgico de longa ação com beta-2 agonista de longa ação.
Alternativa: sem ordem de preferência, podendo ser usada isoladamente ou em associação com as medicações descritas anteriormente
Anticolinérgico de curta ação e/ou beta-2 agonista de curta ação ou
Teofilina.
C – Pacientes pouco sintomáticos e com alto risco de exacerbação
1ª escolha: sem ordem de preferência
Corticoide inalatório + beta-2 agonista de longa ação ou
Anticolinérgico de longa ação.
2ª escolha
Anticolinérgico de longa ação + beta-2 agonista de longa ação.
Alternativa: sem ordem de preferência, podendo ser usada isoladamente ou em associação com as medicações descritas anteriormente
Inibidor da fosfodiesterase ou
Anticolinérgico de curta ação e/ou beta-2 agonista de curta ação ou
Teofilina.
D – Pacientes muito sintomáticos e com alto risco de exacerbação
1ª escolha: sem ordem de preferência
Corticoide inalatório + beta-2 agonista de longa ação ou
Anticolinérgico de longa ação.
2ª escolha: sem ordem de preferência
Corticoide inalatório + anticolinérgico de longa ação ou
Corticoide inalatório + beta-2 agonista de longa ação + anticolinérgico de longa ação ou
Corticoide inalatório + beta-2 agonista de longa ação +inibidor de fosfodiesterase ou
Anticolinérgico de longa ação + beta-2 agonista de longa ação ou
Anticolinérgico de longa ação +inibidor de fosfodiesterase.
Alternativa: sem ordem de preferência, podendo ser usada isoladamente ou em associação com as medicações descritas anteriormente
Carbocisteína ou
Anticolinérgico de curta ação e/ou beta-2 agonista de curta ação ou
Teofilina.
A figura 2 resume essas orientações listando as 1as e as 2as escolhas para cada nível.
45 - Qual o papel dos broncodilatadores no tratamento da DPOC estável?
Os broncodilatadores constituem-se na base do tratamento dos pacientes sintomáticos. Podem ser usados conforme a necessidade em pacientes pouco sintomáticos (nível A), ou de forma regular nos pacientes mais sintomáticos ou com pior função pulmonar (níveis B, C e D).
Os broncodilatadores atuam principalmente reduzindo o tônus muscular liso, com isso aumentando o calibre das vias aéreas e facilitando o esvaziamento pulmonar, o que reduz a hiperinsuflação em repouso e durante o exercício. Melhoram assim a dispneia e a tolerância ao exercício, melhorando a qualidade de vida.
46 - Quais as particularidades dos beta-2 agonistas no tratamento da DPOC estável?
Promovem broncodilatação por relaxamento do músculo liso a partir do estímulo de receptores beta-2 adrenérgicos, com aumento do AMP cíclico. A duração do efeito varia entre os diferentes medicamentos, de 4 a 6 h para salbutamol, fenoterol e terbutalino, 12 h para formoterol e salmeterol, 24 h para indacaterol, olodaterol e vilanterol (este disponível apenas em associação com fluticasona). Apesar da disponibilidade de algumas substâncias por via oral ou parenteral, a via inalatória deve ser sempre a primeira opção. Em pacientes em uso regular do broncodilatador, os de longa duração são preferíveis.
Os principais efeitos colaterais são taquicardia (mais raramente outras taquiarritmias), tremores e hipopotassemia (sobretudo com o uso concomitante de diuréticos).
47 - Quais as particularidades dos anticolinérgicos no tratamento da DPOC estável?
Promovem broncodilatação ao bloquearem a ação da acetilcolina sobre os receptores muscarínicos. A duração do efeito varia de 6 h para o ipratrópio a 24 h para o tiotrópio.
O efeito colateral mais comum é a ocorrência de boca seca, eventualmente com “gosto metálico”. Sintomas prostáticos já foram descritos em alguns pacientes e o uso por nebulização pode precipitar crise de glaucoma caso a medicação atinja diretamente o olho. A possível associação entre o uso de anticolinérgico com maior risco de eventos cardiovasculares em pacientes com DPOC precisa ser melhor investigada.
48 - Quais as particularidades das xantinas no tratamento da DPOC estável?
Não existe consenso se há benefícios em se associar uma xantina ao tratamento da DPOC estável, visto que sua potência broncodilatadora é inferior à dos beta-2 agonistas e à dos anticolinérgicos e os efeitos colaterais são mais comuns e mais sérios. Existe o potencial de efeitos anti-inflamatórios e de redução do risco de fadiga muscular, mas sem comprovação definida.
Os eventos adversos dependem dos níveis séricos, determinados não só pela dose da medicação, mas também por uma série de interações com medicamentos, doenças e hábitos, tornando o controle do tratamento difícil, com necessidade de monitorização laboratorial periódica. Os efeitos colaterais mais comuns são cefaleia, insônia, tremores, vômitos, pirose, mas pode haver arritmias e crises convulsivas.
49 - Quais as particularidades dos corticoides inalatórios (CI) no tratamento da DPOC estável?
Os CI estão indicados para pacientes com DPOC que apresentam exacerbações frequentes ou VEF1
Os eventos adversos mais comuns com o uso crônico de CI são rouquidão, candidíase oral e adelgaçamento e escoriações da pele. Eles parecem aumentar o risco de pneumonia e há o potencial de aumentarem a perda mineral óssea.
50 - Os corticoides sistêmicos estão indicados no tratamento da DPOC estável?
Não. Não há benefícios comprovados com o uso desses medicamentos na DPOC estável; por outro lado, eles associam-se a frequentes e graves eventos adversos: osteopenia e osteoporose, catarata, glaucoma, hipertensão arterial, diabetes, dislipidemias, mioptia, adelgaçamento e escoriações da pele, entre outros.
51 - Quais as particularidades dos inibidores da fosfodiesterase 4 (PDE4) no tratamento da DPOC estável?
O roflumilast, inibidor da PDE4 liberado para o tratamento da DPOC, atua inibindo a quebra do AMP-cíclico intracelular. Está indicado para pacientes muito sintomáticos e com alto risco de exacerbação (nível D) e que já estejam em uso de broncodilatador de longa ação, associado ou não a corticoide inalatório. Redução da frequência das exacerbações parece ser seu principal benefício.
Os principais eventos adversos são: náuseas, redução do apetite e emagrecimento, diarreia, dor abdominal, cefaleia e insônia. Eles são precoces e tendem a melhorar com a continuação do tratamento. Vale a pena lembrar que o roflumilast não pode ser associado com as xantinas.
52 - Quais as particularidades dos mucolíticos e antioxidantes no tratamento da DPOC estável?
Não há recomendação para o uso de mucolíticos no tratamento da DPOC. A N-acetilcisteína e a carbocisteína, descritas como mucolíticos, têm também ação antioxidante e já foram associadas a redução de exacerbações em pacientes com DPOC tratados com corticoide inalatório. Apesar deste possível efeito, não há consenso dos benefícios dessas medicações e elas não são recomendadas de forma rotineira.
53 - Quais as indicações para a terapia substitutiva de alfa-1 antitripsina?
A terapia substitutiva de alfa-1 antitripsina tem indicação restrita, devendo o paciente preencher os seguintes critérios de inclusão:
Fenótipo de alto risco (PiZZ ou PiZNulo);
Níveis plasmáticos menores que 11 mmol/L;
Espirometria com distúrbio obstrutivo;
Idade maior ou igual a 18 anos;
Não tabagista ou ex-tabagista;
Adesão ao tratamento.
Por tratar-se de uma condição rara e com tratamento dispendioso e complexo, ela deve ser idealmente conduzida em centros de referência com experiência. A terapia de substituição é venosa, em regimes semanais, quinzenais ou mensais, com dose de 60 mg/kg/semana ou 250 mg/kg/mês.
54 - Quais são as medidas não farmacológicas importantes para o tratamento da DPOC?
As principais medidas farmacológicas na DPOC são:
Educação sobre a doença;
Reabilitação pulmonar;
Avaliação nutricional;
Vacinação;
Oxigenoterapia;
Tratamentos cirúrgicos.
55 - Por que se deve educar os pacientes a respeito da DPOC?
Embora a educação do paciente em relação à DPOC não melhore sua função pulmonar e sua capacidade de exercício, ela aumenta a capacidade de lidar com a doença e, consequentemente, a qualidade de vida relacionada à saúde.
É vital que os pacientes com DPOC compreendam a natureza de sua doença, os fatores de risco para sua progressão, seu papel no tratamento e a função dos profissionais de saúde para se alcançar ótimas condutas e desfechos de saúde. A educação deve ser delineada às necessidades e ao ambiente de cada paciente, ser interativa, direcionada a melhorar a qualidade de vida, fácil de ser seguida e apropriada às habilidades intelectuais e sociais do paciente e dos que cuidam dele.
Várias estratégias educacionais específicas têm melhorado a adesão do paciente ao tratamento. Na DPOC, adesão não se refere apenas ao fato do paciente tomar seu medicamento corretamente. Ela abrange também uma série de tratamentos não-farmacológicos, como por exemplo, manter um programa de exercícios após ter frequentado um programa de reabilitação pulmonar, tentar e manter a cessação do tabagismo e usar adequadamente aparelhos como nebulizadores, dispositivos inalatórios, espaçadores e concentradores de oxigênio.
56 - O que é reabilitação pulmonar e quando ela está indicada na DPOC estável?
A seguinte definição foi retirada do Documento de Reabilitação da American Thoracic Society e da European Respiratory Society, de 2006:
“Reabilitação pulmonar é uma intervenção multiprofissional, integral e baseada em evidências para pacientes com doenças respiratórias crônicas que estão sintomáticos e frequentemente têm suas atividades da vida diária diminuídas. Integrada ao tratamento individualizado do paciente, a reabilitação pulmonar é delineada para reduzir sintomas, otimizar o estado funcional, aumentar participação, reduzir custos dos cuidados a saúde, por meio da estabilização ou reversão das manifestações sistêmicas da doença”.
Pacientes em qualquer estádio da DPOC podem beneficiar-se com a reabilitação pulmonar e deveriam ser encaminhados ao programa. O habitual é o paciente ser encaminhado em uma fase avançada da doença. Os grupos especializados em reabilitação têm feito esforços para mudar esta atitude do médico e de outros profissionais da área de saúde respiratória, incentivando-os a encaminharem os pacientes em fases menos avançadas da doença. Assim, no nosso ponto de vista, a reabilitação está indicada tão logo o paciente fique consciente de sua incapacidade e seja feito o diagnóstico, independente do estádio de progressão da DPOC.
O acesso a programas formais de reabilitação pulmonar pode ser difícil em determinadas localidades. Assim, o médico que assiste o paciente com DPOC deve entender que o simples fato de estimular o indivíduo a realizar atividades físicas regularmente (exemplo: caminhadas) trará benefícios significativos para o paciente. Em linhas gerais, recomendam-se caminhadas de 30 minutos 5 vezes por semana, ou 50 minutos 3 vezes por semana.
Os principais objetivos da reabilitação pulmonar são reduzir os sintomas, melhorar a qualidade de vida e aumentar a participação física e emocional do paciente nas atividades diárias. Para saber mais veja o Tema Reabilitação Pulmonar.
57 - Qual a importância da avaliação nutricional na DPOC?
A avaliação nutricional habitualmente está incluída no programa de reabilitação. Pacientes desnutridos devem ser orientados em relação à ingesta calórica necessária. Não há consenso sobre os benefícios dos suplementos alimentares (ex. creatina) ou de esteroides anabolizantes sobre desfechos clínicos importantes. Por outro lado, a presença de sobrepeso ou obesidade também tem efeito negativo sobre os sintomas e a qualidade de vida e os mesmos devem ser combatidos.
58 - Quais vacinas estão indicadas para pacientes com DPOC?
Os pacientes com DPOC devem ser vacinados anualmente contra gripe. Tal conduta é capaz de reduzir significativamente as exacerbações graves e os óbitos, sendo considerada evidência A.
Os portadores de DPOC também devem receber a vacina contra o pneumococo. O uso da vacina anti-pneumocócica reduz significativamente a morbidade e a mortalidade em indivíduos com idade acima de 65 anos ou entre aqueles com idade inferior a 65 anos e com VEF1
Os pacientes com DPOC podem, e também devem ser vacinados contra tétano e difteria e hepatite B, como todos os demais indivíduos.
59 - Quando está indicada a oxigenoterapia domiciliar prolongada na DPOC estável?
O uso do oxigênio por portadores de DPOC com hipoxemia é uma medida capaz de reduzir a progressão da doença, com impacto significativo na morbi-mortalidade. A oxigenoterapia domiciliar prolongada está indicada na presença de um dos seguintes critérios:
PaO2 £55 mmHg ou SaO2 £88 % com ou sem hipercapnia;
PaO2 entre 55 mmHg e 60 mmHg, ou SaO2 de 88%, se houver evidência de hipertensão pulmonar, edema periférico sugerindo insuficiência cardíaca congestiva ou policitemia (hematócrito > 55%).
Os pacientes que apresentam queda da saturação arterial periférica de oxigênio apenas durante o exercício podem se beneficiar do seu uso durante a atividade física.
O objetivo principal da oxigenoterapia é elevar a PaO2 basal ao nível do mar e em repouso para no mínimo 60 mmHg e/ou produzir uma SaO2 de no mínimo 90%, o que irá preservar a função dos órgãos vitais e minimizar a vasoconstrição hipóxica na circulação pulmonar, que pode culminar em cor pulmonale.
É importante ressaltar que o efeito benéfico da oxigenoterapia sobre a sobrevida na DPOC foi demonstrado em indivíduos que utilizaram o oxigênio por no mínimo 15 horas por dia. Assim, os pacientes devem ser orientados a utilizar o oxigênio por períodos iguais ou superiores a este. Para saber mais veja o Tema Oxigenoterapia.
60 - Qual o procedimento para os pacientes com DPOC com uso contínuo de oxigenoterapia ao viajarem em aviões?
Embora viagens aéreas sejam seguras para a maioria dos pacientes com insuficiência respiratória crônica que estão em uso de oxigênio prolongado, os pacientes devem ser instruídos a aumentar o fluxo em 1-2 L/min durante o vôo. O ideal é que eles monitores a saturação de oxigênio com oxímetro, mantendo-a acima de 90%.
Cuidado maior deve ser tomado em pacientes com comprometimento do transporte de oxigênio, como os portadores de insuficiência cardíaca ou anemia. Além disso, deve-se recomendar repouso durante o vôo, visto que rápidas caminhadas pelo corredor podem desencadear dessaturação.
61 - Existe indicação de suporte ventilatório em pacientes com DPOC na fase estável?
Embora a ventilação não-invasiva (VNI) seja amplamente usada para tratar exacerbações da DPOC, seu papel na doença estável não está bem definido. Alguns estudos mostraram que, em comparação com a oxigenoterapia isolada, o acréscimo da VNI pode diminuir a retenção de CO2 e melhorar a dispneia em pacientes mais graves. Assim, embora a VNI não possa ser recomendada para tratamento de rotina em pacientes com insuficiência respiratória crônica devido à DPOC, sua combinação com a oxigenoterapia pode ser considerada em casos avançados selecionados.
62 - Quais as opções de tratamento cirúrgico da DPOC?
São elas:
Cirurgia redutora de volume pulmonar;
Bulectomia;
Redução de volume pulmonar com procedimentos broncoscópicos;
Transplante de pulmão.
63 - O que é a cirurgia redutora de volume pulmonar?
Trata-se de um procedimento cirúrgico em que partes do pulmão são ressecadas para reduzir a hiperinsuflação, o que torna os músculos respiratórios geradores de pressão mais eficientes ao melhorar sua condição mecânica (medida pela relação comprimento/tensão, curvatura do diafragma e área de aposição). Além disto, a cirurgia redutora de volume pulmonar aumenta a pressão de retração elástica pulmonar e assim melhora o fluxo expiratório.
A cirurgia redutora de volume pulmonar está indicada para pacientes com enfisema de lobos superiores e baixa capacidade de exercício. Benefícios não foram observados, em comparação com o tratamento clínico, em pacientes que apresentavam outras distribuições de enfisema ou alta capacidade para exercícios antes do tratamento.
A cirurgia está formalmente contra-indicada em pacientes com DPOC com difusão e VEF1 abaixo de 20% do seu valor previsto pela alta mortalidade nos primeiros 30 dias. Mais informações estão contidas no Tema Cirurgia Redutora do Volume Pulmonar no Enfisema.
64 - O que é a bulectomia no tratamento da DPOC?
Ressecção cirúrgica de uma grande bolha que esteja comprimindo o parênquima pulmonar adjacente e que não contribua para as trocas gasosas. A bulectomia pode ser realizada por toracoscopia. Em pacientes cuidadosamente selecionados, este procedimento é eficiente em reduzir a dispneia e melhorar a função pulmonar.
Bolhas podem ser removidas para aliviar sintomas locais como hemoptise, infecção ou dor torácica e permitir a re-expansão de região pulmonar comprimida. Esta é a indicação usual para pacientes com DPOC. Ao considerar o possível beneficio da cirurgia é crucial estimar o efeito da bolha no pulmão e a função da área não bolhosa.
Tomografia do tórax, gasometria arterial e teste de função pulmonar completo são essenciais antes de tomar qualquer decisão a respeito da conveniência para ressecção de uma bolha.
Capacidade de difusão normal ou minimamente reduzida, ausência de hipoxemia significante e evidência de redução regional da perfusão com boa perfusão no restante do pulmão são indicações de que o paciente provavelmente irá se beneficiar da cirurgia. Entretanto, hipertensão pulmonar, hipercapnia e enfisema grave não são contraindicações absolutas para bulectomia.
Alguns pesquisadores recomendam que as bolhas devam ocupar 50% ou mais do hemitórax e produzir deslocamento nítido do pulmão para que se indique a cirurgia.
65 - Qual a indicação para transplante pulmonar no paciente com DPOC?
Em pacientes com DPOC muito avançada e selecionados apropriadamente, o transplante pulmonar tem mostrado melhorar a qualidade de vida e a capacidade funcional. Os critérios recomendados pelo GOLD 2015 para encaminhamento do paciente para fila de transplante são:
Escore BODE entre 7 e 10;
Pelo menos 1 dos seguintes outros:
História de exacerbação que evoluiu com hipercapnia (PaCO2 >50 mmHg);
Hipertensão pulmonar;
Cor pulmonale;
VEF1
Diagnóstico resolvido por componentes: quando deveria ser utilizado?
Component resolved diagnosis: when should it be used? (Diagnóstico resolvido por componentes: quando deveria ser utilizado?) Luengo O, Cardona V. Clin Transl Allergy. 2014 Sep 8;4:28. doi: 10.1186/2045-7022-4-28. eCollection 2014.
Abstract:
The knowledge on molecular allergy diagnosis is continuously evolving. It is now time for the clinician to integrate this knowledge and use it when needed to improve the accuracy of diagnosis and thus provide more precise therapeutic and avoidance measures. This review does not intend to comprehensively analyze all the available allergen molecules, but to provide some practical clues on use and interpretation of molecular allergy diagnosis. The potential role of component resolved diagnosis in circumstances such as the indication of allergen immunotherapy, pollen polysensitization, food allergy, latex allergy or anaphylaxis, is assessed. Interpreting the information provided by molecular allergy diagnosis needs a structured approach. It is necessary to evaluate single positivities and negativities, but also to appraise "the big picture" with perspective.
Comentários de Ataualpa P.Reis:
O conhecimento do diagnóstico molecular da alergia está aumentando continuamente. É necessário que o clínico integre este conhecimento e o utilize quando necessário para melhorar a acurácia do diagnóstico e fornecer medidas terapêuticas e de exclusão mais precisas. Esta revisão não analisa completamente todos os alérgenos moleculares, mas fornece algumas dicas práticas sobre a utilização e interpretação do diagnóstico molecular da alergia.
O diagnóstico por componentes pode ser utilizado na indicação da imunoterapia alérgica, sensibilização múltipla (pólen e alimentos), alergia alimentar (avaliação de risco e de co-fatores), alergia a látex ou anafilaxia.
Anafilaxia
Dados epidemiológicos demonstram que os co-fatores (exercícios, álcool, antiinflamatórios, etc) são relevantes em até 39% dos casos de anafilaxia por alimentos em adultos. A alergia a trigo induzida por exercício é a que melhor caracteriza estes casos e está classicamente relacionada à sensibilização à ômega-5 gliadina. As proteínas transportadoras de lípedes não específicas (nsLTP) também são consideradas importantes co-fatores para alergia alimentar, principalmente relacionada aos vegetais, oleaginosas e cereais, na população mediterrânea. Pacientes com história de reação anafilática relacionada à co-fatores podem ser investigados quanto à presença de imunoglobulina E sérica (sIgE) para nsLTP (especialmente Pru p 3, mas também Tri a 14) e para ômega-5 gliadina.
Em pacientes com história de reação anafilática tardia (3-6 horas após ingestão) para carnes de mamíferos, a sIgE para galactose-alfa-1,3-galactose (alfa-gal) deve ser investigada. Tem sido sugerido que picadas de carrapato sejam os responsáveis por desenvolvimento de sIgE para alfa-gal.
O diagnóstico por componentes múltiplos e a sIgE podem ser utilizados para casos de anafilaxia idiopática.
Alergia ao látex
O diagnóstico por componentes permite diferenciar os pacientes apenas sensibilizados ao látex e aqueles com verdadeira alergia ao látex. Pacientes sensibilizados apenas ao Hev b 8 são assintomáticos à exposição ao látex.
Sensibilização aos múltiplos alérgenos alimentares
Reações alérgicas a frutas e vegetais pode ser resultado de uma sensibilização primária a alimentos ou a inalantes. Em geral, a reatividade cruzada é atribuída à alérgenos lábeis (por exemplo, PR-10 ou profilinas) e associada com reações orais leves, enquanto que os alérgenos resistentes ao calor e à proteólise, estão geralmente associados com reações sistêmicas além das reações locais e com sensibilização primária pela via oral (por exemplo, proteína de estoque e nsLTP).
Avaliação de risco na alergia alimentar
A avaliação por componentes permite detectar os pacientes com maior risco de reações graves. Os principais componentes são aqueles relacionados à nsLTP e proteínas de estocagem.
Interpretar a informação fornecida pelo diagnóstico molecular necessita de uma abordagem estruturada. É necessário avaliar pontos positivos e negativos, mas também avaliar o cenário como um todo em perspectiva.
Effect of allergen avoidance and nasal topical corticosteroid in patients with persistent allergic rhinitis.
Efeito do controle ambiental e corticóide nasal
Ataualpa P. Reis1, Luciana Reis2, José Augusto N. Machado3
Federico Montealegre4
1-Professor Convidado de Pós Graduação em Imunologia da UFMG e da Santa Casa de Belo Horizonte, MG.
2-Médica Estagiária
3-Professor de Pós Graduação em Imunologia da Santa Casa de Belo Horizonte
4-Professor-Escola de Medicina de Ponce ,Ponce, Puerto Rico,USA.
Ataualpa P. Reis- Av. Bandeirantes 1764-CEP 30315000- Belo Horizonte,MG
Tel-31-3221-9900 Fax 31-32242433. Email: ataualpapreis@@gmail.com
Resumo
Objetivos: O propósito deste estudo foi determinar os níveis dos alérgenos ambientais, promover seu controle agressivo, administrar corticóide tópico nasal em crianças portadoras de rinite alérgica persistente e verificar o seu efeito no controle da patologia.
Métodos: Estudo clinico aleatório com 62 crianças com rinite alérgica e asma leve persistente (VEF1> 80% do previsto) foi conduzido. Os participantes, foram alocados aleatoriamente para um grupo de tratamento com terapia tópica nasal em combinação com medidas agressivas para controle do ambiente ou um grupo controle com terapia tópica nasal sem estas medidas. Além disto, ambos os grupos usaram triancinolona tópica nasal continuamente pelo período de estudo. Testamos se esta intervenção e o uso de corticóide nasal teve algum efeito nos escores de sintomas da rinite, no pico de fluxo inspiratório nasal e no nível de alérgenos ambientais durante período de 6 meses.
Resultados: Das 62 crianças, 26 não cumpriram os critérios de inclusão e 6 tiveram descontinuação do tratamento. Melhora significativa foi observada no grupo de tratamento em relação aos sintomas clínicos e nas medidas do pico de fluxo inspiratório nasal (Peak Flow Inspiratório Nasal) em associação com a redução dos níveis de alérgenos ambientais. Houve também melhora menos acentuada dos sintomas clínicos e das medidas do pico de fluxo inspiratório nasal no grupo controle, mas não houve melhora dos níveis de alérgenos ambientais.
Conclusão: Os resultados indicam que medidas agressivas de controle ambiental e o uso simultâneo de corticóide tópico nasal em pacientes com rinite alérgica persistente melhoram os sintomas clínicos, o fluxo inspiratório nasal e os níveis de alérgenos ambientais.O uso somente do corticóide tópico nasal pode também melhorar menos acentuadamente os sintomas clínicos e a obstrução medida por fluxos inspiratórios nasais.
Descritores: controle ambiental, rinite, corticóide nasal, pico de fluxo inspiratório nasal.
Abstract
Objectives: The purpose of the study was to determine the environmental allergens, to promote intensive home control measures and simultaneously to use intranasal steroid in children with persistent allergic rhinitis to verify if this could reduce this pathology.
Methods: Children (62) with clinical persistent allergic rhinitis and mild persistent asthma (FEV1>80% of predicted) were randomly allocated to an aggressive house dust avoidance treatment group and a control group with no intervention . All patients in both groups used a triancinolone nasal spray continuously throughout the study period. We tested whether the intervention and nasal spray corticosteroid had an effect on the rhinitis symptoms scores, peak nasal inspiratory flow and in the home allergens determination levels during 6 months period.
Results: From 62 children, 26 do not fulfill the inclusion criteria and 6 were dropped from treatment. Significant improvements were seen in the treatment group in symptoms scores, and in peak inspiratory flow parameter measurements in association with reduction of antigen determination in their homes. A minor improvement was seen in the control group for the symptoms scores and peak inspiratory nasal flow rates but no reduction of environmental antigens occurred.
Conclusions: The results indicates that aggressive dust mite avoidance measures and the simultaneously use of intranasal steroid in patients with persistent allergic rhinitis had a positive impact in symptoms scores, inspiratory nasal flow and in the environmental allergens levels. The isolated use of the nasal topical corticosteroid had also a minor positive impact in the symptoms scores and inspiratory nasal flow.
Descritores: environment control, rhinitis, nasal corticosteroid, peak nasal inspiratory flow
Introdução:
Rinite alérgica persistente (RAP) é caracterizada por sintomas constantes de obstrução nasal, espirros, prurido e coriza aquosa. Estudos epidemiológicos têm demonstrado que, em média, 40% das crianças podem apresentar sintomas de RAP1.Segundo o Consenso Brasileiro sobre Rinites de 2.000 a prevalência da rinite alérgica no Brasil é de 33% em escolares de 6 a 7 anos e de 34% na faixa etária de 13 a 14 anos2.Vários estudos mostram a forte correlação entre exposição à alérgenos ambientais, especialmente ácaros, fungos e proteínas de animais domésticos, e desenvolvimento de patologia alérgica respiratória3-6. De acordo com o Consenso Brasileiro sobre Rinites2 o tratamento da rinite alérgica deve incluir controle e higiene ambiental, imunoterapia e farmacoterapia.Os indivíduos com rinite alérgica não somente sofrem com o desconforto dos seus sintomas mas também podem freqüentemente desenvolver sinusites7 e asma8 e diagnóstico e terapia precoce podem minimizar esta marcha atópica alérgica9. O controle do meio ambiente por higienização agressiva tem se mostrado terapia bastante eficiente de controlar doença alérgica 10 e o uso de corticóide nasal também é efetivo em aliviar os sintomas da RAP como se demonstrou para beclometasona 11, budesonida12, flunisolida13, propionato de fluticasona14, mometasona15 e triancinolona 16.
Na prática clínica utilizamos de rotina o controle ambiental, os antihistamínicos orais simples ou associados aos descongestionantes, os corticóides tópicos nasais e, às vezes, a imunoterapia para o tratamento da rinite alérgica persistente do tipo leve a moderado. Na rinite persistente grave podemos ainda lançar mão de outros recursos terapêuticos tais como os antileucotrienos os corticóides orais 17 .
Neste estudo investigamos se a associação de intervenção agressiva no ambiente domiciliar do alérgico, com a pretensão de reduzir sua exposição alergênica, e o uso concomitante e prolongado por 6 meses de corticóide nasal em crianças pode alterar a presença dos sintomas da rinite alérgica persistente(RAP).
Métodos e Casuística
Um total de 62 crianças foram recrutadas para participar do estudo. Destes um total de 36 crianças (idade entre 5 e 15 anos) portadoras de RAP e asma leve persistente foi incluído no estudo, duplo cego, aleatório e em paralelo por 6 meses de duração. O protocolo de estudo foi realizado de acordo com a Declaração de Helsinki, sendo que todos os pacientes foram esclarecidos e aceitaram com declaração de consentimento escrita ou verbal por seus pais ou guardiões legais, antes de entrarem no estudo. Os critérios de inclusão foram: diagnóstico clínico de RAP leve a moderada de acordo com a classificação do ARIA Workshop Report (Allergic Rhinitis and Its Impact on Asthma)17 e testes cutâneos positivos a dois ou mais alérgenos ambientais. Os critérios de exclusão foram: pacientes que usaram corticóide nasal, oral, inalado ou intramuscular durante as últimas 4 semanas anteriores ao estudo , pacientes clinicamente instáveis, com infecções do trato respiratório superior, sinusite infecciosa ou exacerbações de asma no período de recrutamento ou durante o estudo.
Depois da visita inicial para seleção, os pacientes participaram de 1 semana de avaliação quando os sintomas nasais, freqüência, uso de medicação e medidas de pico de fluxo inspiratório nasal(PFIN) foram anotadas.Ao fim deste período foram reavaliados e, se estáveis, foram alocados de maneira aleatória nos grupos experimentais para o período de tratamento. Após a inclusão as crianças foram distribuídas em 2 grupos: ativo com 20 crianças em que as medidas agressivas de controle ambiental foram executadas e grupo controle(16 crianças) em que estas medidas não foram executadas.Todas as crianças usaram o corticóide nasal triancinolona durante todo o período de estudo na dose de 1 jato (55 mcg) em cada narina à noite.Também foram permitidas usar medicação broncodilatadora por inalação oral de resgate (salmutamol-SOS) em episódios de asma. Todas foram instruídas para anotar os sintomas diariamente bem como realizaram a espirometria nasal. Estas avaliações foram repetidas a cada 2 meses de intervalo até o final do estudo.
Como medidas agressivas de controle ambiental no grupo ativo foram incluídas simultaneamente : uso de capa impermeável em uma das faces nos colchões e travesseiros, limpeza da casa com pano úmido ou aspiração com aspirador de pó com filtro HEPA ou receptáculo de água, retirar carpetes e pisos acarpetados, uso de poltronas e outros móveis apenas se impermeáveis, lavagem semanal de lençóis e outros tecidos do quarto com água quente a 56 °C, exposição máxima do ambiente à luz solar, evitar brinquedos de pano ou com pelos, aplicar água sanitária em locais de umidade.
A variável primária foi o escore nasal e as secundárias foram as dosagens dos alérgenos ambientais e o pico de fluxo inspiratório nasal. O estudo foi aprovado pelo Conselho de Ética.
Dosagens dos alérgenos ambientais
Os alérgenos dos ácaros ambientais foram pesquisados através de amostras de poeira colhidas seguindo um protocolo de coleta usando-se um aspirador de pó Eletrolux modelo Vac.A-10 aplicado na superfície de 4 áreas predeterminadas: quarto, colchões, sala de TV, tapetes e carpetes.A aspiração era realizada durante 2 minutos em uma área de 1 metro quadrado em cada uma das áreas escolhidas.O material coletado nas 4 áreas foi colocado em frasco apropriado, misturado a 10 ml de tampão e lacrado.Esta solução era sacudida e extraída por 5 minutos e estocada em geladeira a 4oC por um máximo de 4 dias até a análise dos alérgenos pelo ensaio específico semiquantitativo do “Rapid Test for Dust Mite”(Indoor Biotechnologies, Ltd, UK)18. O resultado do nível de alérgenos foi expresso como negativo, nível baixo, moderado e alto, sendo que baixo corresponde a aproximadamente 0.2 μg /g de poeira; médio a 0.2-1.0 μg /g poeira; alto > 1 μg /g de poeira .Uma equipe foi treinada para a coleta do material que era rotulado em código e o pesquisador das amostras não conhecia o código até a abertura dos resultados.
Testes cutâneos.
Os testes cutâneos foram realizados por punturas e com extratos glicerinados que foram adquiridos da IPI-ASAC do Brasil S/A(International Pharmaceutical Immunology-São Paulo) e puntores plásticos descartáveis da IPI-ASAC do Brasil.A bateria de alérgenos padronizados incluiu Dermatophagoides pteronyssinus, D. farinae, Blomia tropicalis, epitélio de cão(Canis familiares), epitélio de gato(Felis domesticus), fungos das espécies Penicillium nonatum, Alternaria alternata, Aspergillus fumigatus e baratas(Blatella germânica e Periplaneta americana). Todos os antígenos usados foram padronizados em unidades biológicas(UBE) e a técnica de puntura padronizada de acordo com Dreborg e Frew19, sendo o critério de positividade a formação de pápula cujo maior diâmetro deve ser igual ou superior a 3mm, com controle negativo igual a zero e controle positivo com histamina(10mg) também superior a 3mm.
Medidas de fluxo inspiratório nasal (PFIN).
As medidas de pico de fluxo inspiratório nasal (PFIN) foram realizadas com um aparelho Mini Wright Peak Flow Meter conectado a uma máscara de anestesia infantil.As crianças eram ensinadas inicialmente a assuar bem as narinas e a seguir inalar o mais rápida e fortemente possível através da mascara e pelas narinas e o melhor de 3 exames executados era gravado.Uma profissional técnica foi treinada pela equipe pesquisadora e foi a única responsável pelas medidas no período de estudo. Os pacientes foram também orientados em como anotar os sintomas nasais diariamente em relação a espirros, prurido, rinorréia aquosa e obstrução nasal, baseados em uma escala de 4 pontos indo de zero a 3. O critério de escores foi de acordo com a tabela I.
Análise estatística foi realizada utilizando-se o teste t Student para as médias independentes.A análise secundária foi realizada utilizando se o teste t Student para as médias pareadas e com desvio padrão da média, sempre analisados em relação à linha basal. Para os resultados em percentual e sem o desvio padrão foi aplicado o teste do Qui-Quadrado. Também foi analisado o coeficiente de correlação entre as medidas do PFIN e as medidas dos níveis de alérgenos nos domicílios utilizando-se o método de Spearman. Nestas avaliações estatísticas usamos os programas de computador SPSS versão 10.0 e o Minitab.LNK versão 13.0 e o nível de significância estatística foi de 5%.
Resultados
Sessenta e dois pacientes foram incluídos no inicio do estudo. Em ambos os grupos alguns pacientes foram retirados.No grupo ativo 4 foram retirados por não completarem as medidas agressivas de controle ambiental e 2 do grupo controle porque apareceram com infecções repetitivas, uso de outras medicações e suspenderam prolongadamente o uso do corticóide nasal. A figura I descreve o fluxo CONSORT de pacientes. As características dos pacientes foram semelhantes com todos da raça branca e com os parâmetros normalmente distribuídos, sendo que os 2 grupos não apresentaram diferenças significantes( tabela II).
Escores nasais
Na análise dos escores totais dos sintomas e dos escores dos sintomas individuais, no inicio do estudo não houve diferença significativa( p> 0.005) tanto para o grupo ativo como para o grupo controle. A seguir nos meses 2, 4 e 6 houve diferenças estatisticamente significante tanto para o grupo ativo quanto para o grupo controle e tanto na somatória total dos sintomas quanto na análise individual de cada sintoma( figuras 2, 3, 4, 5, 6) , mostrando desfecho favorável nos 2 grupos. Quando se comparou a somatória total dos sintomas nos 2 grupos houve diferença significativa para o grupo ativo apenas nos meses 4 e 6 (p 0.05)(figura 6).
Pico de fluxo inspiratório nasal (PFIN).
Na análise das alterações dos picos de fluxos inspiratórios houve um aumento médio em relação à linha básica de 90( ± 5) L/min para 120 ( ± 8) L/min no grupo ativo no mês 2 e de 92 (± 6)L/min para 107 (± 3) L/min no grupo controle. No mês 4 houve aumento para 125 (± 6) L/min no grupo ativo e para 112 (± 2)L/min no grupo controle. No mês 6 o aumento foi para 128(±5) L/min no grupo ativo e para 113(± 4) L/min no grupo controle (p
O coeficiente de correlação entre o PFIN e das medidas de alérgenos ambientais nas casas com altas concentrações alergênicas mostra forte correlação negativa( r= - 0.949 com nível p
Níveis dos alérgenos
O estudo dos níveis de alérgenos dos ácaros ambientais pelo método semiquantitativo foi categorizado como baixo (0.2 microgramas/g de poeira coletada); médio (0.2 a 1.0 mcg/g de poeira e alto (> de 1.0 mcg/g de poeira) e mudança em relação à linha basal inicial para categoria mais baixa ocorreu em 50% no grupo ativo e 21.42% no grupo controle passaram para categoria mais alta ao final do mês 2.No mês 4, 75 % do grupo ativo migrou para mais baixa e no grupo controle 14.29% migraram para mais alta. No mês 6 permaneceu a migração de 75% do grupo ativo para categoria mais baixa e permaneceu a migração de 14.29% para categoria mais alta, sendo que outros 14.29% migraram para categoria mais baixa no grupo controle(p 0.05) mostrando que não houve aqui um desfecho favorável. Portanto a redução dos níveis de alérgenos nos lares com intervenção agressiva foi bastante evidente e durante todo o período de estudo, enquanto que nos lares sem a intervenção agressiva a dosagem dos alérgenos não apresentou maior alteração e não houve evidência de redução ( figura 8 ).
O coeficiente de correlação entre o PFIN e das medidas de alérgenos ambientais nas casas com altas concentrações alergênicas mostra forte correlação negativa( r= - 0.949 com nível p
Discussão
De acordo com os Consensos Internacionais e o Brasileiro sobre o tratamento da asma este tratamento deve incluir o controle ambiental o uso de beta 2 agonistas conforme a necessidade e eventualmente o corticóide inalado 20,21.O último Consenso Brasileiro sobre Rinites aconselha que no tratamento da rinite alérgica leve a moderada se deve incluir o controle ambiental, uso de antihistamínicos tópicos ou orais e corticóide nasal2.
Neste trabalho em que avaliamos o resultado de rotina clássica preconizado para pacientes com RAP e asma leve persistente onde incluímos o controle ambiental, o uso de beta 2 agonistas de acordo com a necessidade e o corticóide nasal para uso prolongado, verificamos o resultado positivo desta conduta para a melhora da RAP e também da asma leve persistente concomitante que estes pacientes apresentavam( Reis,AP- dados não publicados e submetidos à publicação).
O controle ambiental é parte muito importante nesta estratégia. Alergia aos ácaros ambientais é a causa mais comum de doença alérgica respiratória na criança e controle ambiental parece ser a maneira mais lógica de tratar a criança com alergia respiratória relacionada aos ácaros. A literatura que suporta esta afirmação é extensa 4,22-28. Neste estudo a exposição antigênica aos ácaros ambientais foi medida em termos de concentração antigênica como mcg/g de poeira. Este método de avaliação tem sido recomendado pelos 3 últimos workshops internacionais e têm sido usado em diversos ensaios e com sucesso 24,29,30. O uso de métodos baseados na técnica de ELISA( ensaio imuno enzimático com anticorpo monoclonal) tem fornecido um índice bastante válido de exposição antigênica e métodos semiquantitativos, como o que usamos neste ensaio, pode ser usado por clínicas, laboratórios, médicos e até por pacientes para controlar e monitorar o nível de concentração antigênica na casa do alérgico 31. Os alérgenos são medidos em amostras de poeira coletadas por aspirador de pó em área de 1m 2 e por 2 minutos em 3 a 4 locais da casa, principalmente quarto, sala de TV, tapetes, carpetes, e mostram boa correlação da quantidade de alérgenos e índice de exposição. O teste é rápido e dá condições ao pesquisador, médico ou paciente de avaliar o índice em alto, moderado ou baixo por simples linhas coloridas que se correlacionam ao grupo 2 dos antígenos de ácaros determinados pelo teste de ELISA.
Neste trabalho demonstramos também que o uso do corticóide nasal triancinolona melhorou de forma estatisticamente significante os sintomas da RAP no grupo ativo com intervenção agressiva de controle no ambiente domiciliar, mas também no grupo controle em que estas medidas não foram executadas e principalmente quando o uso se torna mais prolongado. O uso do corticóide nasal para tratamento da RAP tem sido reconhecido como efetivo há anos 32,33. Na última década os corticóides tópicos têm se mostrado como a forma mais eficaz do tratamento farmacológico para RAP. Para uso regular e profilático são considerados como os de menor risco para efeitos sistêmicos secundários e daí considerados de primeira linha para o tratamento da RAP 17,34. Recentemente vários trabalhos também demonstraram a eficácia dos corticóides tópicos nasais em melhorarem a obstrução nasal através de rinomanometria e medidas de fluxos inspiratórios nasais 35-37. O PFIN tem sido demonstrado como método confiável de medir a obstrução nasal quando comparado a rinomanometria anterior e posterior 38,39. Neste trabalho também demonstramos que o uso profilático e constante por 6 meses no grupo controle teve efeito positivo sobre a obstrução demonstrada pelo aumento do PFIN e houve correlação negativa entre o sintoma obstrutivo e o fluxo, sendo que isto já ocorreu com 2 meses de tratamento e se manteve constante durante todo o período.
A conclusão final do estudo é de que o controle ambiental e o uso de corticóide tópico nasal em crianças por um período de 6 meses são capazes de reduzir a concentração antigênica nos lares dos pacientes, melhorar os sintomas da RAP e reduzir a obstrução nasal através da melhora dos picos de fluxo inspiratórios nasais(PFIN).
As limitações do estudo foram a impossibilidade ética de não termos um controle sem o uso do corticóide nasal que decidimos ser a mínima terapia de suporte aos pacientes.


Alocados
Intervenção descontinuada (n=4)
Não preencheram os requisitos de controle ambiental
Intervenção descontinuada (=2)
Episódios de infecções repetitivas
Seguimento

Analisados n=16)
Analisados n=14
Análise


A chegada do frio e a baixa umidade do ar, são os principais desencadeador de doenças, como gripes e resfriados, asmas, bronquites, pneumonias, rinites alérgicas, sinusites e asma. Por possuírem sintomas muito parecidos, essas enfermidades podem ser facilmente confundidas. Crianças e idosos são os mais afetados, mas com alguns cuidados é possível minimizar os efeitos que essas doenças geram na saúde neste período do ano.
Vamos então ao esclarecimento das doenças de inverno:
— Gripes e resfriados: embora tenham sintomas aparentemente semelhantes, a gripe e o resfriado são doenças diferentes. O resfriado dura entre quatro e cinco dias, mas pode se prolongar por até duas semanas. Provoca coriza, obstrução nasal, tosse, dor de cabeça, dor de garanta, febre baixa e espirros. É transmitido pelo contato direto entre pessoas. O indivíduo atacado continua firme e consegue realizar suas atividades habituais.Analgésicos e antitérmicos podem aliviar os sintomas.
A gripe, causada pelo vírus influenza, é mais grave e costuma ter duração mais longa. Além dos sintomas do resfriado, provoca febre alta de instalação abrupta, dores pelo corpo e fadiga. Se não diagnosticada e tratada corretamente, a gripe pode desencadear complicações como pneumonias e comprometimento dos brônquios.
— Asma: comum em crianças, mas também presente em adultos, é uma inflamação do pulmão e das vias aéreas, caracterizada por chiados no peito, tosse e sensação de falta de ar.
— Bronquite: inflamação dos brônquios que impede a chegada do ar aos pulmões e muito semelhante a asma. Seus principais sintomas são tosse seca com chiado seguida por tosse com catarro.
— Dor de ouvido ou otite: muito comum em crianças e, normalmente, causada por vírus e bactérias que infectaram a garganta e migraram até o ouvido.
— Pneumonia: é uma infecção aguda dos pulmões causada por bactérias, vírus ou fungos. Ocorre quando há falha nas defesas do organismo e pode surgir após uma gripe ou crise de bronquites mais severas.
— Rinite: é a mais comum das doenças alérgicas, causada pela inflamação ou irritação da mucosa do nariz. Os principais sintomas são espirros, coriza, coceira e entupimento do nariz. Muito semelhante a gripe e resfriados. A diferença principal é que as alergias permitem ao indivíduo levar vida normal enquanto as infecções por vírus geralmente debilitam e tiram a vontade de trabalho, estudo e concentração.
— Sinusite: é a inflamação das cavidades do crânio em torno do nariz, causada por alergias ou infecções virais e bacterianas que provocam dor de cabeça, inchaço nas pálpebras, nariz entupido, secreção nasal e dor nos olhos.
— Alergias: são reações causadas por reação a alguns elementos como ácaros ambientais, poeira ambiental, pelos de animais, mofo, entre outros. Os sintomas para a identificação de alergias vão desde um espirro , coriza aquosa , entupimento coceiras e tosses.
Como prevenir?
— Fazer a vacinação anual contra gripe, que diminui a gravidade da doença e as chances de complicações por óbito. Todas as pessoas e de todas as idades devem usar a vacina, embora o Governo só forneça gratuitamente a uma faixa de maior risco de complicações.
— Se estiver doente evite em dar as mãos para outras pessoas para não contamina-las
— Limpar as mãos com água e sabão depois de tossir ou espirrar, após usar o banheiro, antes de comer e antes de tocar os olhos, boca e nariz.
— Evitar tocar os olhos, nariz ou boca após contato com superfícies que podem estar contaminadas porque o doente pegou
— Proteger com lenços a boca e o nariz ao tossir ou espirrar ou fazê-lo no braço e não nas mãos que vai pegar em outros locais
— No inicio da gripe ou resfriado é possível matar os vírus jogando soro fisiológico na mucosa nasal, por spray, pois os vírus não suportam o pH básico do soro
— Evitar aglomerações e ambientes fechados ( deve-se manter os ambientes ventilados)
— Já em relação as alergias e asma elas são durante todo o ano e recomenda-se:
• Manter os ambientes secos e abertos, permitindo a circulação do ar e a entrada dos raios de sol, capazes de destruir os ácaros e fungos
• Incentivar as crianças a brincar ao ar livre, agasalhando-as no tempo de frio
• Encapar colchões, travesseiros e almofadas com plástico ou tecidos impermeáveis
• Trocar a roupa de cama pelo menos uma vez por semana, lavando-a em água quente
• Usar cobertores antialérgicos, lavando-os regularmente e deixando ao sol para secar
• Evitar plantas, animais de estimação, bichinhos de pelúcia, tapetes ou carpetes, livros e brinquedos acumulados no quarto das crianças
• Retirar as cortinas ou usar aquelas de tecido sintético, mais finas, curtas e presas por argolas para facilitar a remoção e a lavagem
• Substituir a vassoura por pano úmido na limpeza diária, afastando as pessoas alérgicas
• Aplicar produtos antimofo ou água sanitária diluída em água em carpetes, frestas, cantos dos móveis, armários
• Não usar inseticidas em spray nem espiral
• Jamais fumar dentro de casa, perto de crianças ou mesmo de adultos alérgicos
ATAUALPA P. DOS REIS-MÉDICO ALERGOLOGISTA e IMUNOLOGISTA TITULADO PELA ASSOCIAÇÃO BRASILEIRA DE ALERGIA E IMUNOPATOLOGIA E PROFESSOR DE POS GRADUAÇÃO CONVIDADO DA UFMG E SANTA CASA DE BELO HORIZONTE
Efeitos do tratamento com corticosteróide nasal e controle do ambiente em crianças portadoras de Rinite Alérgica e Asma Brônquica
Effect of nasal topical corticosteroid and allergen avoidance in children with allergic rhinitis and asthma
Controle do ambiente e corticosteróide nasal em asma
Ataualpa P. Reis1, Luciana Reis2, José Augusto N. Machado3
1-Professor de Pós Graduação em Imunologia da Santa Casa de Belo Horizonte e da Universidade Gama Filho, MG.
2-Médica estagiária
3-Professor de Pós Graduação em Imunologia da Santa Casa de Belo Horizonte
Ataualpa P. Reis-Avenida do Contorno 4852-CEP 30-110100 - Belo Horizonte, MG
Tel-31-3221-9900 Fax 31-3225-2433 Email: [email protected]
Resumo
Objetivos: A exposição domiciliar a altos níveis de alérgenos do ambiente tem sido relacionada à rinite alérgica e asma e uma intervenção global de controle do ambiente , bem como o uso de corticosteróide tópico nasal, pode ajudar a melhorar as duas patologias. O estudo teve como objetivo primário determinar os efeitos clínicos deste tratamento e como objetivo secundário verificar a redução dos alérgenos ambientais e a redução da asma destes pacientes.
Métodos: 62 crianças com rinite alérgica persistente e asma leve persistente (VEF1> 80% do previsto) foram alocadas randomicamente para um grupo de tratamento com medidas globais para controle do ambiente e um grupo controle sem estas medidas. As medidas agressivas de controle global do ambiente consistiram no uso de capas impermeáveis aos ácaros nos colchões e travesseiros, limpeza e aspiração das poeiras, lavagem regular dos tecidos das camas, evitar carpetes e móveis estofados. Além disto, ambos os grupos usaram triancinolona nasal continuamente pelo período de estudo. Observamos durante um período de seis meses , por ensaio duplo cego, se esta intervenção bi facetada teve algum efeito, primariamente, na redução dos sintomas clínicos e secundariamente no nível de alérgenos do ambiente e nas provas de função pulmonar (VEF1 e Peak Flow).
Resultados: Desfecho favorável foi observado no grupo de tratamento em relação aos sintomas clínicos e nas medidas do pico de fluxo expiratório (Peak Flow) em associação com a redução dos níveis de alérgenos do ambiente. As medidas do VEF1 não melhoraram e houve também desfecho favorável, porém menos acentuado, nos mesmos parâmetros no grupo controle.
Conclusão: Os resultados indicam que medidas globais de controle do ambiente e o uso simultâneo de corticosteróide intranasal em pacientes com rinite alérgica persistente e asma leve persistente têm impacto positivo sobre a asma.
Descritores: controle ambiental, asma, rinite, corticóide nasal
Abstract
Objectives: Home exposure to high level of house allergens has been shown to be related to rhinitis and asthma and global allergen control as well as intranasal use of corticosteroids can reduce both conditions.The primary purpose of the study was to determine the clinical effect of this treatment e secondarily to verify the reduction of environmental allergens and whether this treatment could reduce asthma.
Methods: Children (62) with clinical persistent rhinitis and mild persistent asthma (FEV1>80% of predicted) were randomly allocated to a global house dust avoidance treatment group and a placebo group with no intervention. The global aggressive intervention for the environment control consisted of the use of mite impermeable covers for mattress and bedding, dusting and vacuuming, regular laundered linen, avoidance of carpets and up-holstered furniture. All patients in both groups used a triancinolone nasal spray continuously throughout the study period. We observed during a period of six months, in a double blind action, whether the intervention and nasal spray had an effect on clinical symptoms and secondarily whether there was any effect on the levels of home antigens on the FEV1 and Peak Flow parameters.
Results: Significant improvements were seen in the treatment group in symptoms scores and Peak Flow measurements in association with reduction of antigen determination in their homes. FEV1determinations did not improve and a minor improvement in the same parameters was seen in the placebo group.
Conclusions: The results indicates that global dust mite avoidance measures and the simultaneously use of intranasal steroid in patients with persistent allergic rhinitis and mild persistent asthma had a positive impact in asthma.
Keywords: environment control, asthma, rhinitis, nasal corticosteroid
Introdução:
A asma é a doença crônica mais comum na criança e a causa mais freqüente é a alergia aos ácaros ambientais e outros alérgenos do domicílio1-3. Vários estudos mostram a forte relação entre exposição aos alérgenos do ambiente, especialmente os ácaros, fungos e proteínas derivada de animais domésticos, e desenvolvimento de patologia alérgica respiratória3-6. Além disto, a forte relação entre níveis de exposição e sintomas de asma, bem como gravidade, têm sido demonstrada4, 7-8.
Por outro lado, a inflamação das vias aéreas superiores e inferiores está fortemente associada, de acordo com o “ARIA Workshop Report (Allergic Rhinitis and Its Impact on Asthma)”9, sendo que de 80% a 90% dos pacientes com asma têm rinite alérgica concomitante e cerca de 40% a 50% dos indivíduos com rinite alérgica têm asma10.
Evidenciando o conceito de que intervenções nas vias aéreas superiores podem influenciar favoravelmente nas vias aéreas inferiores, o uso prolongado de corticosteróide intranasal pode proteger contra exacerbações da asma11, bem como reduz hiperreatividade brônquica e melhora os sintomas asmáticos12-14.
Neste estudo investigamos se a associação de intervenção agressiva global no ambiente domiciliar do alérgico, com a pretensão de reduzir sua exposição alergênica, e o uso concomitante e prolongado por seis meses de corticosteróide intranasal em crianças portadoras de rinite alérgica pode alterar a presença e as manifestações de asma.
Pacientes e Métodos
Um total de sessenta e duas crianças (idade entre cinco e quinze anos) portadoras de rinite alérgica persistente e asma leve persistente foi recrutado para participar do estudo. Destas trinta e seis foram incluídas no estudo, duplo cego, aleatório e em paralelo e com seis meses de duração. O protocolo de estudo foi realizado de acordo com a Declaração de Helsinque, sendo que todos os pacientes foram esclarecidos e seus pais ou guardiões legais aceitaram e assinaram o termo de consentimento escrito ou verbal antes de sua admissão.
Os critérios de inclusão foram: diagnóstico clínico de rinite alérgica persistente de acordo com a classificação do II Consenso Brasileiro sobre Rinites15, testes cutâneos positivos a dois ou mais alergenos do ambientes (principalmente ácaros), presença de asma leve persistente (com VEF1 acima de 80% do previsto) de acordo com os critérios de classificação do “Guidelines for the Diagnosis and Management of Asthma-2002” e da IV Diretrizes Brasileiras para o Manejo da Asma-200616-17. Os critérios de exclusão foram: pacientes que usaram corticosteróide nasal, oral, inalado ou intramuscular durante as últimas quatro semanas anteriores ao estudo, pacientes clinicamente instáveis, com infecções do trato respiratório superior, sinusite infecciosa ou exacerbações de asma no período de recrutamento ou durante o estudo.
Depois da visita inicial para a seleção, os pacientes participaram de uma semana de avaliação quando os sintomas, freqüência, uso de medicação, medidas de capacidades respiratórias e pico de fluxo expiratório (PeakFlow) foram anotados.Ao fim deste período foram reavaliados e, se estáveis, foram alocados de maneira aleatória nos grupos experimentais para o período de tratamento. Após a inclusão as crianças foram incluídas em dois grupos: ativo com 20 crianças em que as medidas agressivas globais de controle do ambiente foram executadas e grupo controle (16 crianças) em que estas medidas não foram executadas.Todas as crianças usaram o corticosteróide triancinolona durante todo o período do estudo na dose de um jato (55mcg) em cada narina à noite.Também foi permitido usar broncodilatador inalado de resgate (salbutamol-SOS) em episódios de asma.Todas foram instruídas para anotar os sintomas diariamente, bem como realizaram a espirometria e as medidas do pico de fluxo expiratório. Estas avaliações foram repetidas a cada dois meses de intervalo até o final do estudo.
Como medidas agressivas globais de controle do ambiente no grupo ativo foram incluídas simultaneamente: uso de capa impermeável nos colchões e travesseiros, limpeza da casa com uso de pano úmido ou aspiração com aspirador de pó com filtro HEPA ou receptáculo de água, retirar carpetes e pisos acarpetados, uso de poltronas e outros móveis apenas se impermeáveis, lavagem semanal de lençóis e outros tecidos do quarto com água quente a 56 oC, exposição máxima do ambiente à luz solar, evitar brinquedos de pano ou com pelos, e aplicar água sanitária em locais de umidade.
A variável primária foi o escore de sintomas clínicos asmáticos e as secundárias foram as dosagens dos alérgenos do ambiente, o VEF1 e o pico de fluxo expiratório (Peak Flow). O estudo foi aprovado pelo Conselho de Ética da Santa Casa.
Dosagens dos alérgenos ambientais
Os alérgenos dos ácaros do ambiente foram pesquisados através de amostras de poeira colhidas seguindo um protocolo de coleta usando-se um aspirador de pó Eletrolux modelo Vac.A-10 aplicado na superfície de quatro locais pré-determinadas: quarto, colchões, sala de TV, tapetes e carpetes.A aspiração foi realizada durante dois minutos em uma área de um metro quadrado em cada uma das áreas escolhidas.O material foi coletado em frasco apropriado, misturado a 10 ml de tampão e lacrado.Esta solução era sacudida e extraída por cinco minutos e estocada em geladeira a 4oC por um máximo de quatro dias até a análise dos alérgenos pelo ensaio específico semiquantitativo do “Rapid Test for Dust Mite” (Indoor Biotechnologies, Ltd, UK)19. Os níveis de alérgenos foram expressos como negativo, nível baixo, moderado e alto, sendo que baixo corresponde a aproximadamente 0.2 μg /g de poeira; médio a 0.2-1.0 μg /g poeira; alto > 1 μg /g de poeira. A equipe foi treinada para coleta do material que era rotulado em código e o pesquisador das amostras desconhecia o código até a abertura dos resultados.
Testes cutâneos
Os testes cutâneos foram realizados por punturas e com extratos glicerinados que foram adquiridos de IPI-ASAC do Brasil S/A(International Pharmaceutical Immunology-São Paulo) e puntores plásticos descartáveis da IPI-ASAC do Brasil. A bateria de alérgenos padronizados incluiu: Dermatophagoides pteronyssinus, D. farinae, Blomia tropicalis, epitélio de cão (Canis familiares), epitélio de gato (Felis domesticus), fungos das espécies Penicillium nonatum, Alternaria alternata, Aspergillus fumigatus e baratas(Blatella germânica e Periplaneta americana). Todos os antígenos usados foram padronizados em unidades biológicas (UBE) e a técnica de puntura foi a padronizada por Dreborg e Frew18, sendo o critério de positividade a formação de pápula cujo maior diâmetro deve ser igual ou superior a 3 mm, com controle negativo igual a zero e controle positivo com histamina (10mg) também superior a 3 mm.
Medidas de espirometria e pico de fluxo expiratório (Peak Flow)
A espirometria foi realizada em todos os pacientes no inicio e a cada dois meses subseqüentes usando o espirógrafo Spiromatic Vitatrace VT 130 SL versão 3.2 (Pro Médico LTDA) e interfaciado a um computador (Dell Dimension-Pentium de 1.80 GHZ) com o programa de software desenvolvido pela Engelógica- Engenharia de Sistemas LTDA.Uma profissional técnica foi treinada pela equipe pesquisadora e foi a única responsável pelas medidas no período de estudo, sendo também a responsável pelas medidas de pico de fluxo expiratório (Peak Flow meter) em um aparelho Wright Peak Flow Meter e o melhor de três exames, calculados após correção de temperatura e pressão barométrica ambiente, foi gravado. Os pacientes foram também orientados em como anotar os sintomas asmáticos diariamente em relação à falta de ar, chiado, tosse, cansaço e perda de sono.
A análise estatística foi realizada utilizando-se o teste t Student para as medidas independentes. A análise secundária foi realizada utilizando-se o deste t Student para as medidas pareadas e com desvio padrão da média, sempre analisados em relação à linha basal. Para os resultados em percentual e sem o desvio padrão foi aplicado o teste do Qui-Quadrado. Também foi analisado o coeficiente de correlação entre as medidas do pico de fluxo expiratório (Peak Flow) e as medidas dos níveis de alérgenos nos domicílios utilizando-se o coeficiente de correlação de Spearman. Nestas avaliações estatísticas usamos os programas de computador SPSS versão 10.0 e o Minitab.LNK versão 13.0 e o nível de significância estatística foi de 5%.
Resultados
Sessenta e dois pacientes foram incluídos no inicio do estudo.Em ambos os grupos alguns pacientes foram retirados. Vinte e seis foram retirados por não completarem os critérios de inclusão e trinta e seis foram alocados para os 2 grupos de estudo.No grupo ativo quatro foram retiradas por não completarem as medidas agressivas globais de controle do ambiente e dois do grupo controle porque apareceram com infecções repetitivas, uso de outras medicações e suspenderam prolongadamente o uso do corticosteróide nasal. A figura 1 descreve o fluxo CONSORT de pacientes.
As características dos pacientes foram semelhantes com todos da raça branca e com os parâmetros normalmente distribuídos, sendo que os 2 grupos não apresentaram diferenças significantes (tabela I)
Não foi objeto deste estudo, mas os sintomas da rinite alérgica melhoraram acentuadamente ao longo dos seis meses em ambos os grupos após o uso do corticosteróide nasal (Reis AP et als: Rev.Bras.Alerg.Imunopatol 2006; 29, 201-209).
Escores asmáticos
Os escores asmáticos foram analisados de acordo com a tabela de pontos de Borg20 em relação à falta de ar, chiado, tosse, cansaço, e perda de sono, sendo que todos eram portadores de asma persistente leve de acordo com a classificação da IV Diretrizes Brasileiras para o Manejo da Asma-200616, apresentando VEF1 acima de 80% do previsto. Na linha basal os sintomas tiveram escore médio 3.1 ± 0.3 pontos e nos meses subseqüentes apresentaram 2.6 ± 0.2; 2.1± 0.4; 1.7 ± 0.3 pontos para o grupo ativo e 2.9 ± 0.2; 2.4 ± 0.3; 2.3 ± 0.2 pontos para o grupo controle (Fig.2).A análise estatística dos meses 2 , 4, e 6 para o grupo ativo em relação à linha basal, apresentou desfecho positivo com significância de p
Pico de fluxo expiratório
A análise do Peak Flow (pico de fluxo expiratório) mostrou aumento médio em relação ao basal e interação ao longo do período de estudo sendo linha basal= 290 ± 49 com aumento para 305 ± 38 L/min no mês 2; no mês 4 houve aumento para 312 ± 32 L/min e houve aumento para 324 ± 38 L/min no mês 6 para o grupo ativo e para o grupo controle a linha basal foi de 282 ± 34 e aumento para 290 ± 28 L/min no mês 2; sendo que no mês 4 houve aumento para 294 ± 30 L/min e aumento para 310 ± 26 L/min no mês 6 . Houve portanto desfecho favorável no grupo ativo no mês 6 (p
A espirometria com medição do VEF1 também foi realizada nestes mesmos intervalos em todos os pacientes do grupo ativo e do grupo controle, mas em relação ao valor basal não houve alteração significativa em ambos os grupos.A medida do VEF1 no grupo controle inicialmente foi de 87% do previsto em média e no grupo ativo 84% do previsto.No mês 6 as medidas médias eram de 84% e 85% do previsto, respectivamente.
Níveis dos alérgenos
O estudo dos alérgenos dos ácaros do ambiente pelo método específico semiquantitativo foi categorizado como baixo (0.2 microgramas/g de poeira coletada); médio (0.2 a 1.0 mcg/g de poeira e alto os acima de 1.0 mcg/g de poeira e mudança em relação aos valores basais iniciais para categoria mais baixa ocorreu em 50% no grupo ativo e 21.42% no grupo controle passaram para categoria mais alta ao final do mês 2. No mês 4, 75 % do grupo ativo migrou para categoria mais baixa e no grupo controle 14.29% migraram para mais alta. No mês 6 permaneceu a migração de 75% do grupo ativo para categoria mais baixa e permaneceu a migração de 14.29% para categoria mais alta, sendo que outros 14.29% migraram para categoria mais baixa no grupo controle (p 0.05) mostrando que não houve aqui um desfecho favorável. Portanto, a redução dos níveis de alérgenos nos lares com intervenção agressiva global foi bastante evidente e durante todo o período de estudo, enquanto que nos lares sem a intervenção agressiva global a dosagem dos alérgenos não apresentou maior alteração e não houve evidência de redução (figura 4).
O coeficiente de correlação das medidas do pico de fluxo expiratório e das medidas dos níveis de alérgenos do ambiente nas casas com altas concentrações alergênicas mostra forte correlação negativa (r= - 0.949 ; p
Discussão
É conhecido que 80 a 90 % dos pacientes com asma têm rinite alérgica e 40 a 50% dos pacientes com rinite alérgica têm asma10.A razão pela qual alguns indivíduos com rinite alérgica desenvolvem hiperreatividade brônquica, enquanto outros não, não é conhecida.Uma possibilidade é que a alta exposição à alérgenos seja importante fator indutor. Sob condições naturais,a hiperreatividade brônquica pode ser induzida por exposição sazonal a alérgenos em indivíduos portadores apenas de rinite alérgica21.Este fenômeno pode também ser reproduzido em laboratório. Um estudo envolvendo 16 indivíduos com rinite alérgica e nenhuma hiperratividade brônquica (
Inúmeros trabalhos consistentemente mostram que o tratamento da rinite alérgica beneficia asma. Embora antihistamínicos sejam geralmente considerados como sem ação sobre a asma, o estudo ETAC (Early Treatment of the Atopic Child) em que cetirizina foi administrada por 18 meses a crianças atópicas de 1-2 anos de idade com testes positivos a ácaros e polens, resultou em aproximadamente 50% de redução de incidência de asma25.Diversos estudos demonstram a eficácia do uso de corticosteróide tópico nasal em pacientes com rinite alérgica intermitente e asma leve. Welsh e cols. em 1987 já demonstraram que pacientes com rinite alérgica em uso de beclometasona ou flunisolida tópicas melhoraram significativamente os sintomas brônquicos26. Corren e cols.em seguida examinaram o efeito de beclometasona intranasal sobre a hiperreatividade brônquica em pacientes com rinite alérgica e asma leve e demonstraram, com o teste de provocação por metacolina, grande melhora da reatividade brônquica27. Outros estudos examinaram o efeito do corticosteróide intranasal em pacientes com rinite alérgica persistente e asma leve. Por exemplo, um deles examinou o uso de budesonida intranasal e demonstrou redução das medidas objetivas de obstrução nasal, sintomas de asma e broncoespasmo induzido por exercício28. Em seguida Watson e cols. examinaram o efeito de beclometasona intranasal sobre os sintomas asmáticos e resposta brônquica a testes de provocação com metacolina, tendo concluído por redução dos sintomas asmáticos e reatividade induzida pela metacolina29. Além disto, estes autores completaram elegantemente o trabalho demonstrando que, beclometasona marcada por radioisótopo e depositada na via intranasal, era encontrado somente com 2% de deposição na área pulmonar, ficando claro que o efeito do corticosteróide era por via nasal e não por via pulmonar. Recentemente autores brasileiros e canadenses demonstraram que triancinolona nasal é capaz de reduzir os marcadores inflamatórios das vias aéreas inferiores quando usados para rinite alérgica em pacientes também portadores de asma30.
De acordo com os Consensos Internacionais e o Brasileiro sobre o tratamento da asma este tratamento deve incluir o controle do ambiente, o uso de agentes beta 2 agonistas conforme a necessidade e o corticosteróide inalado em doses baixas16-17.O último Consenso Brasileiro sobre Rinites aconselha que no tratamento da rinite alérgica se deve incluir o controle do ambiente, uso de antihistamínicos tópicos ou orais e corticosteróide nasal15.
Neste trabalho em que avaliamos o resultado da rotina clássica preconizada para pacientes com rinite alérgica persistente e asma leve persistente onde incluímos o controle ambiental, o uso de agente beta 2 agonista de acordo com a necessidade e o corticosteróide nasal para uso prolongado, verificamos o resultado positivo desta conduta não só sobre rinite alérgica (Reis AP et als: Rev.Bras.Alerg.Imunopatol 2006; 29, 201-209) mas também sobre a asma leve concomitante que estes pacientes apresentavam. Quando medimos o pico de fluxo expiratório (Peak Flow) houve desfecho favorável no grupo tratado mas também no grupo controle que usou apenas o corticosteróide nasal por um período de seis meses, mas esta melhora ocorreu somente no 6° mês de estudo, demonstrando melhor resultado principalmente para o uso mais prolongado (Fig 3). Devido a pouca biodisponibilidade da triancinolona nasal, é muito pouco provável que nossos resultados sejam devido à ação sistêmica deste composto e sim pela ação antiinflamatória do corticóide sobre as células inflamatórias e citocinas locais que têm repercussão em toda a extensão da árvore respiratória que se constituem em um trato único.
O controle do ambiente é parte muito importante nesta estratégia. A alergia aos ácaros ambientais é a causa mais comum de doença alérgica respiratória na criança e o controle do ambiente parece ser a maneira mais lógica de tratar criança com alergia respiratória relacionada aos ácaros.A literatura que suporta esta afirmação é extensa31-38. Custovic et cols descreveram a correlação entre a exposição aos ácaros, reatividade a metacolina e diminuição do VEF1 em adultos39.Chang- Yeung et cols notaram que crianças asmáticas sensíveis aos ácaros mostravam uma relação positiva entre os sintomas asmáticos e nível de alérgeno do ambiente e relação negativa entre Peak Flow e nível de ácaros40.Investigadores australianos demonstraram que mudanças na concentração alergênica nas camas correlacionaram positivamente com hiperreatividade brônquica à histamina e sintomas asmáticos33.Investigadores europeus relataram que o uso de capas impermeáveis aos ácaros nas camas, combinado com o uso de filtros, melhora a hiperreatividade brônquica, embora não tenham verificado melhora no VEF1, Peak Flow ou sintomas asmáticos34.Murray e Ferguson , estudando crianças asmáticas com controle do ambiente em que incluíram capas impermeáveis no travesseiro e colchão, ausência de carpetes e brinquedos de pelúcia ou outros que retêm poeira, verificaram menos sintomas de asma, menor uso de medicação e melhora no Peak Flow36.Walshaw e Evans, avaliando adultos asmáticos com ambiente controlado usando capas impermeáveis, lavagem semanal dos tecidos das camas, limpeza ou remoção de carpetes, remoção de poltronas estofadas, verificaram melhora no Peak Flow, relação VEF1/CVF, hiperreatividade brônquica à histamina, mas não ao VEF1 isolado, quando compararam ao grupo controle37. Neste estudo a exposição antigênica aos ácaros do ambiente foi medida pela concentração antigênica em mcg/g de poeira. Este método de avaliação tem sido recomendado pelos três últimos workshops internacionais e tem sido usado em diversos ensaios e com sucesso37,41,42. O uso de métodos baseados na técnica de ELISA (ensaio imuno enzimático com anticorpo monoclonal) tem fornecido um índice bastante válido de exposição antigênica e métodos semiquantitativos, como o que usamos neste ensaio, podem ser usados por clínicas, laboratórios, médicos e até por pacientes para controlar e monitorar o nível de concentração antigênica na casa do alérgico43. Os alérgenos são medidos em amostras de poeira coletadas por aspirador de pó em área de 1 m2 e por 2 minutos em três a quatro locais da casa, principalmente quarto, sala de TV, tapetes, carpetes, e mostram boa correlação da quantidade de alérgenos e o índice de exposição.O teste é rápido e dá condições ao pesquisador, médico ou paciente de avaliar o índice em alto, médio ou baixo por simples linhas coloridas que se correlacionam ao grupo dois dos antígenos de ácaros determinados pelo teste de ELISA.
A grande limitação deste estudo está no fato de não termos um grupo controle sem o uso do corticosteróide nasal, devido a problemas éticos.
A conclusão final do estudo é de que o controle do ambiente e o uso de corticosteróide tópico nasal em crianças por um período de seis meses são capazes de reduzir a concentração antigênica nos lares dos pacientes e melhorar a sua asma, demonstrado pela redução dos sintomas e do pico de fluxo expiratório (Peak Flow).






De: ataualpa pereira dos reis [mailto:[email protected]]
Enviada em: quarta-feira, 9 de fevereiro de 2011 10:38
Para: [email protected]
Assunto: Re: MATERIA SOBRE ALERGIAS
- Quais são os alérgenos mais comuns?
- Está acontecendo uma evolução terapêutica?
- No Brasil, a alergia mais comum entre as criança é a asma, este dado também corresponde ao índice de alergias entre adultos?
- O choque anafilático é ainda causa de muitas mortes ?
- No ambiente de trabalho, o ar-condicionado é considerado um dos vilões para as pessoas que sofre de alergia,verdade ou mito?
-O que é necessário para o diagnóstico adequado das doenças alérgicas?
Cara christiane
1- quais são os alérgenos mais comuns.
Em anexo vc. Vai encontrar o documento 1 que é um levantamento desta questão em belo horizonte que fizemos e publicamos. O comum são os ácaros domiciliares d. Pteronyssimus, d. Farinae e b.tropicalis, que respondem por 83% dos alérgenos causadores de doenças alérgicas respitatórias que também são as mais comuns em alergia. Em seguida vêm os fungos atmosféricos, os restos de barata e os pelos animais. Preste atenção que pólens em nosso meio é muito raro ao contrário de outros países não tropicais.
2- está acontecendo uma evolução terapêutica?
Sim e enorme. A indústria cada vez mais sintetiza moléculas com alta especificidade para medicamentos cada vez mais eficazes. A imunoterapia molecular com anticorpos cada vez mais dirigidos contra o alvo e por alta tecnologia de engenharia genética ,já está no armamentarium terapeutico atual.
Cada vez estamos mais caminhando para o estudo da epigenética ( influência do meio ambiente no dna ),com caracterização fenotípica que permitirá caracterizar individualmente os pacientes para que o tratamento com a farmacologia seja orientada especificamente. Por exemplo, alguns asmáticos respondem bem a corticoterapia enquanto outros não. Como separá-los? Mapeamento de dna e introduções epigenéticas no dna.
3- se a epidemiologia das crianças é a mesma do adulto
Olha christiane, os levantamentos epidemiológicos no brasil que têm validação internacional foram realizados com crianças de 7 a 8 anos e 13 a 14 anos e são os que te mandei. Quanto aos adultos não existem dados epidemiológicos validados mas, estima-se que a asma seja a mais comun também e podendo se dizer que atinge cerca de 20% da população brasileira com grandes variações de acordo com cidades diferentes e regiões diferentes
4- o choque anafilático e´causa de muitas mortes?
Sim é. Ele pode ocorrer por veneno de picada de abelhas, marimbondos e formigas; reação a alguns anestésicos; reação a alguns medicamentos; e raramente a alimentos como é o caso do camarão.
Não existe um tratamento que possa prevenir o choque, mas existem medicamentos de abortar a crise e a orientação aos pacientes quanto a cuidados de evitar a exposição.
5- quanto ao ar condicionado é um mito. Ele não provoca reações alérgicas em ninguém. O que pode acontecer é que pessoas alérgicas são mais sensíveis as mudanças térmicas que ele provoca e daí a pessoa dizer que o ar provoca crise alérgica .se o ar não tem boa manutenção ele pode acumular fungos e bactérias e espalhar pelo ar quando é ligado e causar infecções e não alergias.
6- o diagnóstico adequado das doenças alérgicas depende do bom conhecimento clínico do especialista em alergia e imunologia que assiste o paciente, de uma adequada investigação da causa através de testes cutâneos de diagnóstico, provas de função respiratória e investigação laboratorial por exames com anticorpos monoclonais específicos para os alérgenos suspeitos de provocar a reação alérgica.
Sem um bom diagnóstico não haverá um bom tratamento. Não vivemos mais no tempo do "achômetro", a medicina tem que ser por evidência científica e não se pode mais tolerar diagnósticos baseados em eu acho que, eu penso, eu tenho a certeza, é bem provável, deve ser, é um inicio,,,etc etc etc
Ataualpa P. dos Reis
O mais importante de tudo é a sua anamnese ou história clínica.
Coleta-se aqui seus sintomas, seus antecedentes de doenças, seus antecedentes familiares, as influências do meio a que você está submetido ,o uso de medicamentos, sua dieta, seu modo de vida e as influências do ambiente de trabalho.
A seguir o médico realiza um exame físico na procura de sinais objetivos e das características do problema, faz ausculta do seu pulmão, verifica detalhes de mucosa em cavidades, procura alterações da normalidade dos tecidos, mede pressão, pulso, temperatura, etc.
Feita a hipótese diagnóstica da patologia o médico parte para a realização de exames complementares para a comprovação ou não da hipótese e tentar chegar a causa do problema. Dentre estes exames cabe ressaltar:
1. TESTES ALÉRGICOS POR INTRADERMO REAÇÃO OU POR PUNTURA
Como a maioria das asmas são de natureza alérgica cabe realizar os testes alérgicos.Estes testes constam de se aplicar na pele substâncias suspeitas de causar o problema.São praticamente indolores e apresentam uma reação de vermelhidão e edema em 15 a 20 minutos e que desaparecem após 1 ou 2 horas sem deixar marcas .Têm grande valor quando se trata de antígenos ou substâncias que penetram no organismo por via inalatória e menor quando se trata de alimentos, drogas, bactérias ou vírus. (PRINCIPAIS CAUSADORES DAS ALERGIAS).
2. PATCH TESTES ALÉRGICOS OU TESTES DE CONTATO
São testes de se aplicar as substâncias na pele e se deixar por 48 horas mantidas no local por artefato próprio. Retira-se após este período e se verifica a reação que também é de vermelhidão, edema e às vezes uma espécie de queimadura local. Por outras vezes, é necessário pedir ao indivíduo que se submeta a exposição de raios solares por cerca de 30 minutos,para que ocorra a reação nas próximas 24 horas e então se faz outra leitura. São testes muito eficientes e que revelam principalmente as alergias aos cosméticos,substâncias de contato,dermatites profissionais. São de pouca valia em Asma e DPOC.
3. RAST, MAST, ELIZA OU TESTES IN VITRO COM ANTICORPOS MONOCLONAIS
Quando o médico não é especialista no assunto estes exames oferecem uma alternativa de valor igual aos testes cutâneos para diagnóstico da causa da Asma.
São testes usados por laboratórios através de material coletado no sangue periférico e utilizando técnicas de detecção dos antígenos por anticorpos monoclonais, específicos para cada substância pesquisada ou por múltiplos grupos de substâncias.Têm a desvantagem de se ter que retirar sangue e não são imediatos como os testes cutâneos que são paralelos ao exame do paciente.São geralmente reservados para os casos de peles de difícil uso ou para crianças muito pequenas em que os testes cutâneos dão pouca reação ou são complicados de se executar. Estes testes embora tenham boa especificidade,não levam qualquer vantagem em relação aos testes cutâneos em relação a sensibilidade e são muito caros.
4. TESTES DE PROVOCAÇÃO
Estes testes são usados para esclarecer diagnóstico duvidoso de Asma.
Nestes testes são usadas as substâncias suspeitas e que vão desencadear exatamente a reação que se pesquisa. Existem os de provocação inespecífica em que se usam agentes capazes de desencadear a reação com determinadas doses e que medem a sensibilidade do indivíduo e os específicos a exatamente ao que se suspeita ser a pessoa alérgica. Os testes de provocação oral são usados quando se trata de alergia alimentar e os testes de provocação nasal ou de broncoprovocação quando se trata de alergia respiratória. Consistem de se mandar ingerir ou inalar o antígeno suspeito e aguardar a manifestação.
Estes testes têm um certo risco de desencadear reações intensas e portanto reservados a profissionais habilitados a controlar estas respostas.
5. EXAMES DE FUNÇÃO RESPIRATÓRIA
Estes exames estão hoje em dia computadorizados e consistem de orientar a pessoa fazer algumas manobras respiratórias em aparelhos capazes de analisar a função normal ou alterada e transmitir ao computador que vai analisar os dados e dar resultados. Aqui o médico consegue analisar o grau do distúrbio e distinguir se é do tipo constritivo ou restritivo. O primeiro é compatível principalmente com asma brônquica e o segundo com bronquites, enfisema pulmonar ou DPOC. Consegue ainda analisar se o distúrbio responde bem a eventual medicação e pode ainda fazer suposições futuras de evolução da patologia. Estes exames são muito usados para se estudar asma brônquica e DPOC e mesmo dar o diagnóstico correto.
TRATAMENTO
BRONCODILATADORES
São usados na Asma Brônquica e na DPOC. Existem em várias formas de uso mas dá-se preferência hoje aos com apresentação em spray pressurizado(bombinhas de aerosol), porque têm menos efeitos colaterais e o efeito é imediato. Portanto são infundados os conceitos superados que provocam taquicardia, aumento da pressão e paradas cardíacas por arritmias o que na verdade ocorre principalmente com os via oral e são devidos a abuso ou excesso de uso. (LINK COM ASMA BRÔNQUICA) Estes medicamentos são usados como sintomáticos e na medida da necessidade (SOS),sendo que espaçadores facilitam o uso. São, no entanto, puramente sintomáticos não atuando na causa do problema. Não devem ser usados de modo continuo em Asma.
Existem os broncodilatadores de ação prolongada (12 ou 24 horas ) e que em DPOC são o tratamento de primeira linha nas formas moderadas e para uso continuo.
CORTICOSTEROIDES
São usados nas reações alérgicas intensas,na asma brônquica,na DPOC, nas inflamações. São medicamentos muito potentes e podem ser usados nas vias oral, injetável ou por spray pressurizado.A via fica na dependência da intensidade e no local do problema .A via oral e a injetável são mais usadas para ataque imediato as reações alérgicas, a inflamação ou uma exacerbação aguda e por um tempo curto, não ultrapassando geralmente a 14 dias, quando passam a ter maiores chances de efeitos colaterais. A via inalatória por spray pressurizado ou por cápsulas de pó inalável, é a mais usada para o tratamento da asma brônquica e geralmente por períodos prolongados por levar a muito menores efeitos colaterais. Existe um tendência moderna de se encarar a asma como uma doença inflamatória crônica associada aos fenômenos alérgicos e daí se preconizar o uso precoce dos corticoides inalados nesta patologia. Os corticoides inaláveis são também usados em DPOC nas formas mais avançadas ( moderada e graves) .
Deve-se evitar ao máximo o uso de corticoides de depósito pela frequente possibilidade de levar aos efeitos colaterais e que são indesejáveis.
ANTIBIÓTICOS E ANTIINFLAMATÓRIOS
Os antibióticos são usados para se combater infecções que podem aparecer e complicar os problemas existentes. São muito importantes nas fases agudas que complicam o enfisema,a bronquite ou a asma. As sinusites crônicas que podem perpetuar as patologias respiratórias devem ser tratadas por antibióticos apropriados e por tempo prolongado, nunca inferior a 3 ou 4 semanas. Nas pneumonias agudas são da maior valia e nunca devem ser usados por tempo muito curto (3 dias) pela possibilidade de não resolver a infecção e criar cepas resistentes. Os anti inflamatórios inalados em asma são o Cromolin e o Nedocromil. Não atuam na fase aguda mas são bastante eficientes na fase crônica e diminuem o uso dos broncodilatadores e dos corticoides, além de serem bastante seguros e quase sem efeitos colaterais. Podem ser combinados com broncodilatadores. Estão cada vez mais em desuso no Brasil.
IMUNOTERAPIA
As vacinas devem ser usadas como parte da estratégia global de tratamento da asma e que inclua os medicamentos e o controle ambiental e nunca isoladamente como tratamento único. Podem ser indicadas por via injetável subcutânea ou por via sublingual. Deve ser sempre indicada com base nos alérgenos detectados pelos testes cutâneos ou pelos exames de sangue específicos, sabendo-se também que são assim bastante eficazes mas se usadas por tempo prolongado. Modernamente se entende o seu efeito por estimular uma população de células linfocíticas denominadas TH1 e diminuir as TH2, conhecidas como responsáveis pelas reações alérgicas, maiores causadoras da asma. Por estes conhecimentos modernos tem-se preconizado o uso precoce de imunoterapia nos 2 primeiros anos de vida quando seria possível dirigir estas populações para o rumo desejado antes que a criança se tornasse definitivamente alérgica.
Está havendo hoje também uma tendência de se indicar vacinas antiinfluenza (causadores de gripes) e antipneumocócicas (causadores de pneumonias) em pessoas mais velhas ou debilitadas, portadoras de Asma ou DPOC.
REFERÊNCIAS:
1. Barnes PJ. Chronic obstructive pulmonary disease. N Engl J Med. 2000;343:269-80
2. IV Diretrizes Brasileiras para o Manejo da Asma-2006- Rev Bras Alerg Imunopatol 29:222-245
3. Guidelines for the Diagnosis and Management of Asthma – NAEPP Expert Panel Report 3; 2007
4. Diagnosis and treatment of asthma in childhood: A PRACTALL consensus report- Allergy 2008 63:5-49
5. Barnes PJ, Pedersen S, Busse WW. Efficacy and safety of inhaled corticosteroid therapy: a systematic review and meta-analysis. Arch Intern Med 1999;159:941.
6. Glolobal Strategy for Asthma Management and Prevention-Updated 2011. www.ginasthma.org
7. Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstrcutive Pulmonary Disease. National Heart, Lung and Blood Institutes. Updated 2011. www.goldcopd.com
8. Tratado de Alergia e Imunologia Clínica 2012. Livraria Atheneu. Editores: Solé D, Bernd LAG, e Rosario Filho N.
Pneumonia é o nome que damos à infecção de um ou ambos os pulmões. Para sermos mais precisos, a pneumonia é a infecção dos tecidos pulmonares e seus alvéolos.
A pneumonia é uma infecção não contagiosa causada habitualmente por bactérias, mas que também pode ser provocada por vírus ou fungos.
O QUE SÃO OS ALVÉOLOS?
Para entender o que é a pneumonia é preciso antes conhecer um pouco a anatomia do pulmão.
Leia o texto e acompanhe a figura abaixo para entender melhor as explicações. O ar que respiramos entra pelo nariz e/ou boca e vai para a traqueia. A traqueia, ao chegar ao nível dos pulmões, bifurca-se, formando os brônquios principais, um para o lado esquerdo, outro para o direito; estes brônquios também se bifurcam, formando os bronquíolos, que por fim, acabam nos alvéolos. Cada vez que ocorre uma bifurcação, as estruturas vão se tornando progressivamente menores.
Os alvéolos, que ficam no ponto final da árvore respiratória, são bolsas microscópicas que estão em contato com a corrente sanguínea. Através deles são feitas as trocas dos gases respirados (oxigênio e gás carbônico). O alvéolo entrega o oxigênio respirado para as hemácias (glóbulos vermelhos) no sangue e recebe delas o gás carbônico produzido pelas células do corpo. Portanto, como todo s sabemos, inspiramos oxigênio e expiramos gás carbônico.

Anatomia pulmonar
Cada um dos pulmões contém milhões de alvéolos. Se pegarmos cada um dos alvéolos e esticarmos lado a lado, a superfície coberta seria de cerca de 75 metros quadrados.
Na pneumonia, os alvéolos ficam cheios de secreções purulentas, impedindo a entrada e saída dos gases. Nestes alvéolos acometidos pela infecção não há troca de oxigênio por gás carbônico. Quantos mais alvéolos acometidos pela pneumonia, mais grave é o quadro. O paciente com pneumonia extensa pode apresentar insuficiência respiratória, precisando ser intubado e acoplado a um respirador artificial para conseguir manter o sangue adequadamente oxigenado.
COMO SE PEGA PNEUMONIA?
A pneumonia pode ser causada, em ordem decrescente de frequência, por: bactérias, vírus, fungos e parasitos.
A maioria das pneumonias são de origem bacteriana. As bactérias que mais habitualmente provocam pneumonia são: Streptococcus pneumoniae, Pseudomonas aeruginosa, Klebsiella pneumoniae, Haemophilus influenzae, Moraxella catarrhalis e Staphylococcus aureus
Na verdade, “pegar pneumonia” não é termo mais apropriado, uma vez que tal expressão passa a ideia de transmissão da doença entre indivíduos. Na grande maioria dos casos, a pneumonia não é uma doença contagiosa como a gripe ou tuberculose.. Você pode entrar em contato com um paciente com pneumonia, que, exceto em situações especiais, não haverá risco de contaminação.
Como então surge a pneumonia? Nossos pulmões são órgãos expostos constantemente a micróbios do ar e da nossa própria flora bacteriana da boca. Nós não ficamos doentes o tempo todo porque o pulmão tem seus próprios mecanismos de defesa, que o mantém livre de germes. Entre estes mecanismos podemos citar o reflexo de tosse, a presença de células do sistema imunológico ao longo de todo trato respiratório e a existência de microscópicos cílios na árvore brônquica que “varrem” os agentes invasores para fora das vias respiratórias.
O desenvolvimento da pneumonia depende da virulência do invasor, da quantidade de micróbios que conseguem chegar aos pulmões e das condições imunológicas do paciente. Em geral, uma pneumonia surge quando um germe agressivo consegue penetrar o trato respiratório e encontra o sistema de defesa comprometido.
Situações triviais podem reduzir as defesas do sistema respiratório. Por exemplo: pacientes que fumam apresentam uma irritação constante de toda árvore brônquica e disfunção dos cílios protetores. As células de defesa pulmonar também são afetadas pelo cigarro e não funcionam tão bem. Tudo isso favorece o aparecimento de infecções respiratórias. Outro exemplo são os pacientes com gripe. A lesão que o vírus da gripe provoca do sistema respiratório também favorece a invasão de bactérias, que se aproveitam da redução da capacidade do paciente de combater os germes que chegam às partes mais interiores do sistema respiratório. Pessoas idosas naturalmente têm seu sistema imunológico mais fraco, o que as coloca sob maior risco de desenvolver pneumonias. Do mesmo modo, pessoas já debilitadas por outras doenças, como insuficiência cardíaca, alcoolismo ou diabetes, também apresentam maiores riscos.
FATORES DE RISCO PARA PNEUMONIA
Os principais fatores de risco para pneumonia são:
– Idade maior que 65 anos.
– Infecções respiratórias virais, como gripe.
– Tabagismo.
– Doenças imunossupressoras ( HIV, transplante, câncer…).
– DPOC (bronquite crônica e enfisema pulmonar
– Usuários de drogas.
– Doentes acamados.
– Pessoas com redução do nível de consciência.
– Hospitalizações prolongadas.
– Pacientes em ventilação mecânica (em uso de respirador artificial).
– Pacientes com outra doença pulmonar prévia (sequelas de tuberculose, bronquiectasias, fibrose cística, etc.)
Pneumonia por aspiração
Um tipo gravíssimo de pneumonia é a pneumonia por aspiração. Ocorre em pessoas que vomitam e logo após aspiram o seu conteúdo. É um tipo de pneumonia comum em pacientes com nível de consciência reduzido, que perdem a capacidade de tossir ou de engolir a própria saliva, fazendo com que as secreções da cavidade oral caiam nas vias respiratórias. A via aérea desta pessoa fica exposta a uma quantidade imensa de micróbios, muito maior do que o habitual, favorecendo o desenvolvimento de pneumonia..
SINTOMAS DA PNEUMONIA
Os sinais e sintomas da pneumonia incluem tosse com expectoração, febre, calafrios, falta de ar, dor no peito quando se respira fundo, vômitos, perda de apetite, prostração e dores pelo corpo. Pode haver presença de sangue misturado ao escarro e a febre da pneumonia é geralmente alta.
É muito comum a pneumonia surgir como complicação de uma gripe. Muitas vezes o paciente acaba atribuindo seus sintomas de pneumonia à gripe, demorando a procurar ajuda médica. É preciso ter atenção a quadros de gripe que não melhoram, ou até pioram progressivamente, principalmente se o paciente for idoso.
Pacientes acima de 60 anos ou com outras doenças, como insuficiência renal, insuficiência cardíaca, cirrose, HIV ou uso de drogas imunossupressoras, podem apresentar um quadro mais discreto, com pouca tosse e nenhuma febre. Às vezes, a pneumonia neste grupo se apresenta apenas com prostração e alterações mentais, como desorientação e confusão mental.
Uma das complicações possíveis da pneumonia é a formação de derrame pleural, que colabora para o surgimento de cansaço e falta de ar.
Nas pneumonias extensas, quando grande parte do tecido pulmonar está acometido, o paciente pode entrar em insuficiência respiratória, sendo necessária a intubação orotraqueal, ventilação mecânica e internação em unidade de terapia intensiva (UTI).
.
Pneumonias atípicas
Existe um grupo de bactérias, entre elas Mycoplasma, Legionella e Clamídia, que causam as chamadas pneumonias atípicas. São formas que podem ter evolução mais lenta e com quadro não tão óbvio de pneumonia.
DIFERENÇAS ENTRE PNEUMONIA E TUBERCULOSE
Muitos pacientes que apresentam um quadro de tosse e expectoração ficam assustados com a possibilidade de terem tuberculose. A diferença está no tempo de evolução da doença. A pneumonia é um quadro agudo que evolui em horas. O paciente fica mal com pouco tempo de doença, procurando atendimento médico já nas primeiras 72 horas de doença. A tuberculose se apresenta como um quadro mais arrastado, com os sintomas piorando gradativamente e o paciente muitas vezes só procura atendimento médico várias semanas depois do início dos sintomas.
DIAGNÓSTICO DA PNEUMONIA
O diagnóstico da pneumonia é feito normalmente com exame físico e uma radiografia de tórax. Análises de sangue podem ajudar, mas não são imprescindíveis. Um bom médico é capaz de diagnosticar uma pneumonia apenas com a história clínica e o exame físico.
A radiografia, por ser um exame barato e amplamente disponível, é normalmente solicitada para confirmação do diagnóstico. Os alvéolos cheios de secreção aparecem como uma mancha branca à radiografia de tórax, como se pode ver na foto ao lado
O hemograma do paciente com pneumonia apresenta uma grande elevação do número de leucócitos, típico de infecções .Nos pacientes mais graves, que necessitam de hospitalização, normalmente tentamos identificar qual é a bactéria responsável pela pneumonia. Podemos pesquisar a bactéria no sangue (através da hemocultura) ou no próprio escarro do paciente. Em casos selecionados pode ser necessária a coleta de secreções diretamente do pulmão, através da broncoscopia.
TRATAMENTO DA PNEUMONIA
As pneumonias são divididas em comunitárias, quando adquiridas no dia-a-dia, e hospitalares, quando surgem em pacientes hospitalizados. A pneumonia hospitalar é mais grave e mais difícil de tratar, pois é normalmente causada por bactérias mais resistentes e acomete pacientes mais fragilizados.
O tratamento das pneumonias bacterianas é feito com antibióticos por no mínimo oito dias. As pneumonias comunitárias podem ser tratadas com antibióticos orais, porém, aquelas que evoluem mal necessitam de internação hospitalar e antibióticos venosos.
As principais drogas usadas para as pneumonias comunitárias são a amoxacilina com ácido clavulânico, azitromicina, claritromicina, ceftriaxona, levofloxacino e moxifloxacino. Esperam-se sinais de melhora a partir do segundo ou terceiro dia de tratamento.
Pneumonias podem facilmente levar à sepse e costumam ser importante causa de morte em idosos e pacientes imunossuprimidos.
Já existe vacina contra a pneumonia estreptocócica, causada pelo Streptococcus pneumoniae, o tipo mais comum. Ela está indicada em crianças e pessoas acima dos 50 anos, mas não evita pneumonias causadas por outros germes.
PEGAR FRIO CAUSA PNEUMONIA?
A história do frio é muito difundida na população, mas apresenta apenas uma pequena parcela de verdade. Como eu já explicado, para se ter pneumonia é necessário uma infecção bacteriana; não basta uma corrente de ar frio para nos infectar.
O que acontece é que no frio (no Brasil poucos lugares fazem realmente frio) o sistema de defesa, principalmente os cílios das vias aéreas, funcionam de modo mais lento, o que favorece a invasão de germes. No inverno as pessoas andam menos na rua e tendem a se aglomerar em locais fechados, favorecendo a transmissão de vírus como o da gripe. Como já referido, infecções respiratórias virais são fatores de risco, principalmente em idosos, para o aparecimento de pneumonia.
Agora, ninguém pega pneumonia porque abriu a geladeira com o corpo molhado ou porque pegou uma chuva saindo do trabalho ou do colégio. Felizmente, nosso sistema imune é suficientemente forte para lidar com situações triviais como estas.
O sistema imunitário ou sistema imunológico ou ainda sistema imune é um sistema de estruturas e processos biológicos que protege o organismo contra doenças. De modo a funcionar corretamente, o sistema imunitário deve detectar uma imensa variedade de agentes, desde os vírus aos parasitas, e distingui-los do tecido saudável do próprio corpo.
Nosso ambiente está repleto de agentes infecciosos como vírus, bactérias, fungos, protozoários, alérgenos ambientais e o sistema imunológico trabalha combatendo estes invasores. O organismo possui vários tipos de barreiras contra os invasores. O tipo de resposta imune do organismo vai depender do invasor e do local da invasão.
Existe um conjunto de barreiras físicas e bioquímicas que impedem que os microorganismos provoquem uma inflamação. São também chamadas de mecanismos de defesa não específicos, pois defendem o organismo de qualquer tipo de invasor.
A principal barreira contra os microorganismos é a pele devido a sua constituição de queratina, que impede a entrada deles. Os mucos revestem as mucosas e normalmente os invasores ficam aderidos nele. Os cílios “varrem” os microorganismos para fora do órgão.
As enzimas contidas na saliva e na lágrima possuem ação bactericida. Algumas enzimas possuem o pH muito ácido, que impede a proliferação de microorganismos na região. No intestino há numerosos microorganismos da flora normal que impedem a proliferação de microorganismos externos, competindo por comida e espaço.
Através da imunidade adquirida, o organismo cria memória imunitária na sequência de uma resposta inicial a um agente específico, o que lhe permite responder de forma mais eficaz a novos ataques pelo mesmo agente. O processo de imunidade adquirida é a base da vacinação.
A resposta imune
Para produzir a defesa, o organismo precisa primeiramente reconhecer o patógeno ou qualquer que seja este invasor. Existem dois tipos de resposta imune: inata e adaptativa.
Resposta imune inata
Quando um microorganismo invade o organismo, um grupo de células fagocitárias vai tentar destruí-los através da fagocitose. Estas células são um grupo de leucócitos: monócitos, macrófagos e neutrófilos. Este tipo de reconhecimento é inespecífico, pois as células fagocitam vários tipos de microorganismos e compreendem a primeira linha de defesa. É uma resposta importante pois se comunica ao mundo exterior e faz uma adaptação do nosso organismo a este mundo.
Caso o patógeno evite a resposta inata, os vertebrados possuem um segundo nível de defesa, o sistema imune adquirido, que é ativado pela resposta inata e através do qual o sistema imunitário adapta a sua resposta durante uma infecção de acordo com a identificação do patógeno. Através da memória imunológica, o corpo memoriza esta resposta, o que permite ao sistema imunitário adquirido realizar ataques cada vez mais rápidos e robustos cada vez que esse mesmo patógeno é detectado.
Resposta imune adaptativa
A resposta imune adaptativa é específica e conta com os linfócitos, que reconhecem especificamente o patógeno invasor. Existem vários tipos de linfócitos que são agrupados em duas categorias: linfócitos B, que produzem anticorpos que se ligam ao antígeno do invasor e os linfócitos T, que estão envolvidos na produção de linfócitos B , auxiliam na fagocitose e podem também ser destruidores do invasor. Existem vários tipos de interação entre os linfócitos e fagócitos.
Células do sistema imune
Linfócitos
Os linfócitos são responsáveis pelo reconhecimento do invasor e produção da resposta imune. São produzidos na medula óssea e timo, que são órgãos linfóides primários ou centrais e migram para o baço, linfonodos e amígdalas, que são tecidos linfóides secundários. Os linfócitos B são produzidos na medula óssea e os linfócitos T migram para maturação no timo.
Linfócitos B: os linfócitos B reconhecem o receptor de superfície do antígeno e transformam-se em plasmócitos, que produzem e secretam anticorpos que se ligam especificamente com o antígeno do invasor. Os linfócitos B ficam concentrados os gânglios linfáticos, prontos para uma reação.
Linfócitos T: os linfócitos T são bastante variados e possuem um número grande de funções. Eles interagem com os linfócitos B. As células T auxiliares (TH) auxiliam os linfócitos B na produção de anticorpos, divisão e diferenciação celular. Os linfócitos T citotóxicos destroem células infectadas do hospedeiro, utilizando um receptor especifico para antígenos das células T (TCR). Os efeitos dos linfócitos T estão relacionados com a liberação de citocinas, que são emissores químicos de sinais para as células.
Fagócitos mononucleares
Os fagócitos têm a função de neutralizar, englobar e destruir as partículas estranhas e microorganismos invasores. São produzidos na medula óssea e sua diferenciação é provocada por citocinas. Quando estas células estão no sangue circulante são chamadas de monócitos, quando estão nos tecidos são chamadas de macrófagos.
Neutrófilos
Os neutrófilos são células fagocíticas e são muito numerosos, compreendendo cerca de 90% dos granulócitos que circulam na corrente sanguínea. É a primeira célula a chegar ao local de defesa e tem vida curta.
Eosinófilos
São células com função de apreender e danificar os invasores, principalmente os parasitas extracelulares grandes. Quando estimulados, eles liberam seus grânulos, liberando toxinas, histaminas e arilsulfatase. Os eosinófilos combatem principalmente os vermes, pois não podem ser fagocitados. As substâncias produzidas também ajudam a diminuir a resposta inflamatória. São também muito efetivos na resposta alérgica do nosso organismo
Basófilos e mastócitos
Estas células estão em quantidades muito pequenas no sangue. Possuem grânulos no citoplasma que produzem inflamação no tecido circundante. Estão também associados com as reações alérgicas.
Plaquetas
As plaquetas estão envolvidas com a coagulação sanguínea e na liberação de mediadores inflamatórios, atraindo leucócitos para a região lesada.
Citocinas
São proteínas ou peptídeos que permitem que as células comuniquem entre si e com outros órgãos durante as respostas imunes. Principais grupos:
Interleucinas: são produzidas principalmente pelas células T e estão relacionadas com a multiplicação dos linfócitos B. Existem vários tipos de interleucinas.
Interferons: estão relacionados com a produção de defesa contra os vírus, mantendo as células em estado de “alerta viral”.
Sistema complemento
É um grupo de proteínas com a função de controlar o processo inflamatório. São produzidas pelo sangue e estão presentes no fígado. Pode ser ativado por anticorpos presentes nas paredes das bactérias (via clássica) ou por moléculas que estão presentes nas bactérias (via alternativa). Esta bactéria é revestida por moléculas do complemento,facilitando a fagocitose.
Anticorpos
Também chamados de imunoglobulinas, são proteínas produzidas pelos linfócitos B que reconhecem antígenos e se ligam especificamente com eles e interagindo com outras células do sistema imune, servindo como um adaptador. Existem cinco classes de anticorpos: IgG, IgA, IgM, IgD e IgE.
Antígenos
Qualquer organismo ou proteína que é reconhecido pelo sistema imune.
Resposta inflamatória
A inflamação inespecífica é uma das primeiras respostas do sistema imunitário à infecção. A inflamação manifesta-se através de vermelhidão, inchaço, sensação de calor e dor localizada, causadas pelo aumento da circulação sanguínea nos tecidos afetados.
Todo o sistema específico se concentra na capacidade das células imunitárias distinguirem proteínas produzidas pelas células do próprio corpo (antigeno "self" - ou seja do próprio organismo), e proteínas produzidas por invasores ou pelas células humanas transformadas p.e. por vírus (antigeno "non-self" - ou seja, que não é reconhecido como sendo do próprio organismo). As células do sistema imune é que vão exercer esta função.
Transtornos da imunidade humana.
O sistema imune é uma estrutura notável que incorpora especificidade, indutibilidade e adaptação. No entanto, ocorrem falhas na defesa, que são classificadas em três grupos genéricos: imunodeficiências, autoimunidade e hipersensibilidades.
As imunodeficiências ocorrem quando um ou mais dos componentes do sistema imunitário estão inativos. A capacidade do sistema imunitário de resposta aos patógenos é menor nas camadas mais jovens e mais velhas da população. A resposta imunitária entra em declínio por volta dos 60 anos de idade devido imunossenescência. Em países desenvolvidos, a obesidade, o alcoolismo e o uso de drogas são as causas mais comuns da insuficiência imunitária. No entanto, a má nutrição é a causa mais comum de imunodeficiência em países em desenvolvimento.
As imunodeficiências também podem ser herdadas ou adquiridas. Um exemplo de imunodeficiência congênita, ou herdada, é a doença granulomatosa crónica, na qual os fagócitos têm dificuldade em destruir os patógenos. A SIDA e alguns tipos de câncer estão na origem de imunodeficiência adquirida.
Autoimunidade é a falha em uma divisão funcional do sistema imunológico chamada de autotolerância, que resulta em respostas imunes contra as células e tecidos do próprio organismo. Qualquer doença que resulte deste tipo de resposta é chamada de doença autoimune. Exemplos famosos incluem a diabetes mellitus tipo 1, lúpus eritematoso sistêmico, síndrome de Sjögren, tireoidite de Hashimoto,doença de Graves e artrite reumatóide.
São doenças que surgem quando a resposta imunitária é efetuada contra alvos existentes no próprio indivíduo. Respostas autoimunes são frequentes, porém transitórias e reguladas. A autoimunidade como causadora de doenças não é frequente, uma vez que existem mecanismos que mantêm um estado de tolerância aos antígenos do próprio organismo. As doenças autoimunes têm etiopatonogênese complexa e multifatorial.
A hipersensibilidade é uma resposta imunitária que danifica os tecidos do próprio corpo. Divide-se em quatro classes (tipos I a IV) com base nos mecanismos envolvidos e no intervalo de tempo da reação hipersensível. A hipersensibilidade do tipo I é uma reação normalmente associada à alergia. Os sintomas podem ser respiratórios, cutâneos ou gastrointestinais. Este tipo I é mediado pela imunoglobulina E, que provoca a degranulação dos mastócitos e dos basófilos quando ligados por um antígeno.
Imunologia dos tumores
Outro papel importante do sistema imunitário é a identificação e a eliminação de tumores. As células modificadas dos tumores expressam antígenos que não estão presentes em células normais. O sistema imunitário interpreta estes antígenos como exteriores e a sua presença leva a que as células imunitárias ataquem as células do tumor. Os antígenos expressos por tumores podem ter várias origens. Alguns são derivados de vírus carcinogênicos, como o vírus do papiloma humano que provoca o cancer do colo do útero, enquanto que outros têm origem nas próprias proteínas do organismo, tendo pouca intensidade em células normais mas atingindo valores elevados nas células dos tumores.
ATAUALPA P. DOS REIS- MÉDICO ALERGISTA E IMUNOLOGISTA E PROFESSOR DE PÓS GRADUAÇÃO EM ALERGIA E IMUNOLOGIA
CID-10: A16, A16.0; A16.1, A16.2, A16.3, A16.4, A16.5, A16.7, A16.8, A16.9
Parte I - Principais conceitos e aspectos clínico-terapêuticos na Tuberculose
1. Definição
Doença infectocontagiosa, de evolução crônica, causada pelo Mycobacterium tuberculosis ou bacilo de Koch, com comprometimento pulmonar e/ou extrapulmonar. No complexo Mycobacterium, são ainda importantes as espécies M. bovis e M. avium intracelulare, esta última em imunodeprimidos.
2. Epidemiologia
Estima-se que um terço da população mundial esteja infectada pelo Mycobacterium tuberculosis (WHO, 2007), sendo 95% dos casos e 98% dos óbitos concentrados nos países em desenvolvimento (MS,SVS,2009).
O Brasil está entre os 22 países responsáveis por esses casos, porém, até o ano de 2007, apresentou uma queda de 26% na incidência e 32% na mortalidade pela doença, que se tornou expressiva a partir de 1999 com a implantação da estratégia de tratamento diretamente observado (DOTS = Directly Observed Treatament Strategy) SBPT, 2009.
Problema adicional é o surgimento de cepas resistentes - tuberculose multirresistente (MDR-TB) – em decorrência de tratamentos incompletos ou mal supervisionados, comprometendo o controle da doença (UNAIDS, 2006). A DOTS objetiva não só reduzir essas ocorrências, como também contribuir para as metas do milênio pactuadas pela Organização das Nações Unidas, de reduzir em 50% as taxas de incidência e mortalidade pela doença até 2015 CONDE, ET AL, 2009.
Neste contexto, destaca-se a infecção pelo HIV, como o mais potente fator de risco para a conversão de tuberculose latente em tuberculose doença, e também a presença do bacilo como acelerador da evolução do portador assintomático para a AIDS (UNAIDS, 2006).
3. Transmissão
Ocorre preferencialmente por via aérea ou digestiva, de forma direta gotículas de Flügge ou beijo); ou indireta aspiração de poeira contaminada, gotículas desidratadas suspensas no ar (núcleos de Wells) (MS,SVS,2009). O meio ambiente é extremamente hostil ao bacilo, onde não se reproduz, sendo o indivíduo bacilífero a principal fonte de contaminação.
Apesar do perfil da tuberculose no Brasil ser mais de transmissão comunitária, foram observadas elevadas taxas de transmissão da doença em escolas médicas, hospitais universitários, serviços de emergência, prisões e casas de saúde psiquiátricas. Neste sentido, a utilização conjunta de medidas administrativas, ambientais e de proteção respiratória, é fundamental para reduzir o risco de infecção nos ambientes com maior concentração de doentes. SBPT, 2009
4. Classificação
4.1 - Período de infecção (Primoinfecção) MS,SVS,2009
Lesão inicial pulmonar associada à adenopatia perihilar ou paratraqueal, que caracteriza o complexo
primário de Hanke. Pode ocorrer, neste momento, uma disseminação linfohematogênica sistêmica.
Cerca de 90% dos indivíduos conseguem bloquear o avanço do processo, permanecendo apenas como infectados.
4.2 - Tuberculose latente ou infecção latente pelo M. tuberculosis MS,SVS,2009; CONDE, et al, 2009; CAVALCANTI, 2010
Corresponde ao período compreendido entre a penetração do bacilo no organismo e o aparecimento da tuberculose doença. É passível de intervenção medicamentosa, hoje denominada “tratamento da tuberculose latente”, em substituição ao termo “quimioprofilaxia”, anteriormente utilizado.
4.3 - Tuberculose primária MS,SVS,2009; FAUCI et al,2010
Decorre da progressão da lesão inicial para doença clínica, a partir do foco pulmonar e/ou ganglionar ou em consequência de disseminação hematogênica. Ocorre em 5% dos primoinfectados.
4.4 - Tuberculose pós-primária MS,SVS,2009; FAUCI et al,2010; CONDE, et al, 2009; CAVALCANTI, 2010
Decorre do recrudescimento de algum foco já existente no organismo (reativação endógena) ou de
exposição a nova carga bacilífera (reinfecção exógena), em geral, tempos depois da primoinfecção.
5. Formas clínicas MS,SVS,2009; FAUCI et al,2010; CONDE, et al, 2009; CAVALCANTI, 2010
5.1 - Tuberculose pulmonar
Dependendo da fase evolutiva da doença, pode apresentar distúrbios ventilatórios restritivos,
obstrutivos, de difusão e/ou de perfusão.
Sinais e sintomas inespecíficos surgem de forma insidiosa, tais como, febre, em geral baixa e vespertina, sudorese noturna, perda de peso, anorexia, mal estar geral e astenia. A maioria dos casos apresenta tosse, inicialmente seca e posteriormente produtiva, com expectoração purulenta, algumas vezes com hemoptóicos, ou mesmo franca hemoptise. Dor pleurítica pode ocorrer em indivíduos com lesões parenquimatosas subpleurais. Pode evoluir com dispnéia e, em situações mais graves, com franca insuficiência respiratória.
5.2 - Tuberculose miliar MS,SVS,2009; FAUCI et al,2010
Decorre da disseminação hematogênica do bacilo. Embora mais frequente em crianças, em sequência à primoinfecção, pode acometer adultos imunocomprometidos, tanto a partir de uma infecção recente, como da reativação de um foco preexistente. O aspecto miliar decorre da formação de pequenos granulomas (1 a 2 mm) disseminados em pulmões e diversos órgãos.
As manifestações sistêmicas são graves e inespecíficas, podendo estar presentes sinais e sintomas
respiratórios, digestivos, hepatomegalia, esplenomegalia, linfadenomegalias, entre outros.
5.3 - Tuberculose extrapulmonar ( Corresponde a 5 a 10 % de todos os casos )
Sistema Nervoso Central: MS, FUNASA, CENEPI, 2004; NUNES et al, 1998a; NUNES et al, 1998b
Pode acometer meninges ou o parênquima cerebral.
Manifesta-se como meningoencefalite de evolução subaguda, cursando quase sempre com febre, irritabilidade, sinais clínicos de hipertensão intracraniana e irritação meníngea, paralisia de pares cranianos e letargia, podendo evoluir para estado comatoso. Tem alta taxa de letalidade e resulta em até 30% de sequelas neurológicas graves e incapacitantes.
- Pleural (FAUCI et al,2010)
É comum ocorrer na tuberculose primária, podendo resultar de propagação contígua à inflamação do parênquima ou, na fase pós-primária, em decorrência de ativação de foco bacilífero no espaço pleural. A intensidade do derrame pode variar de leve, com resolução espontânea, a mais intenso, com macicez à percussão e ausência de sons respiratórios, acompanhando-se de febre, dor torácica e dispnéia.
- Pericárdica (FAUCI et al,2010)
Frequente em imunodeprimidos, se deve à progressão direta de um foco primário dentro do pericárdio, à reativação de um foco latente ou à ruptura de um linfonodo adjacente. As taxas de letalidade chegam a 40%. O início pode ser subagudo, embora forma aguda, com dispnéia, febre, dor retroesternal e atrito pericárdico, seja possível. Pode ocorrer derrame pericárdico, com 3
sintomas cardiovasculares e sinais de tamponamento cardíaco. Sem tratamento, a tuberculose pericárdica geralmente é fatal. Mesmo tratada, pode evoluir com complicações, dentre as quais se inclui pericardite constritiva crônica.
- Ganglionar: MS, FUNASA, CENEPI, 2004; PAES et al, 2006
Acomete com frequência cadeia cervical, sendo geralmente unilateral. Pode também acometer primariamente gânglio(s) de cadeia axilar, inguinal, supraclavicular ou submandibular. A evolução é lenta, superior a três semanas, com gânglios de consistência endurecida, podendo ou não fistulizar (escrófula ou escrofuloderma).
- Genitourinária (FAUCI et al,2010)
Pode envolver qualquer porção do trato urinário e mais de 1/3 dos pacientes apresenta doença pulmonar concomitante. Os principais sintomas são: aumento da frequência urinária, disúria, nictúria, hematúria, dor abdominal e em flancos. Em alguns casos, no entanto, a tuberculose urinária pode evoluir sem sintomas, sendo descoberta apenas quando já existe extensa lesão destrutiva.
A tuberculose genital é mais frequente em mulheres, acometendo principalmente as trompas e endométrio, podendo acarretar infertilidade, dor pélvica e alterações menstruais. Em homens acomete o epidídimo, produzindo massa ligeiramente macia que pode fistulizar, além de orquite e prostatite. Cerca de metade dos casos cursa com doença concomitante no trato urinário.
- Osteoarticular
Além das manifestações sistêmicas da doença, tende a apresentar dor no segmento atingido, atitude antálgica, alterações da marcha, limitação de movimentos, paraplegias e gibosidade.
Geralmente é secundária à localização pulmonar e quase sempre ocorre a partir do primeiro ano após a primo-infecção, por via linfo-hematogênica. (MS, FUNASA, CENEPI, 2004; CABRAL et al, 2005)
Acomete mais frequentemente a coluna vertebral (Mal de Pott), quase sempre com envolvimento de dois ou mais corpos vertebrais adjacentes. Pode haver também comprometimento de articulação coxofemoral e joelho. (FAUCI et al,2010)
- Gastrointestinal (FAUCI et al,2010)
Forma incomum. Embora qualquer parte do trato gastrintestinal possa ser afetado, o íleo terminal e
ceco são os locais mais envolvidos. Dor abdominal (às vezes semelhante ao associado à apendicite), edema, obstrução, hematoquesia e massa palpável no abdome são achados comuns,
assim como febre, perda de peso, anorexia e sudorese noturna.
- Cutânea (FAUCI et al,2010)
As manifestações cutâneas da tuberculose incluem a infecção primária, devido à inoculação direta, além de abscessos, úlceras crônicas, escrofuloderma, lúpus vulgar (doença latente com nódulos, placas e fissuras), lesões miliares, e eritema nodoso.
- Ocular (FAUCI et al,2010)
Pode cursar com coriorretinite, uveíte, panoftalmite e hipersensibilidade dolorosa relacionada a
conjuntivite flictenular.
- Otorrinolaringológica (FAUCI et al,2010)
Forma rara, mas que pode cursar com otorréia, perfuração da membrana timpânica e perda auditiva ou nasofaringite de duração prolongada, que não responde às medidas terapêuticas habituais.
- Outras localizações possíveis (mamária, nasal, laríngea, entre outras).
6. Diagnóstico (MS, SAS,DAB, 2008, Bacha, 2005, MS,SVS,2009, CONDE, et al, 2009, CAVALCANTI, 2010)
6.1 - História e exame físico
- Quadro febril a esclarecer (febre vespertina, em geral baixa )
- Tosse produtiva por 3 semanas ou mais ( com ou sem hemoptóicos )
- Emagrecimento, sudorese noturna e/ou dor torácica
- Comunicantes de casos de tuberculose
- História de tratamento anterior para tuberculose
- Confinamento em instituições; doenças debilitantes; imunossupressão
- Uso de drogas; moradores de rua; trabalhadores da área de saúde
- Exame físico variável de acordo com a forma clínica
6.2 - Exames complementares
6.2.1 - Exame bacteriológico (MS, SAS,DAB, 2008, Bacha, 2005, MS,SVS,2009)
Materiais: escarro, lavado brônquico, lavado gástrico, líquido pleural, líquido pericárdico, líquido peritoneal, fragmento de biópsia de tecidos diversos, líquor, urina e fezes.
- Baciloscopia direta para pesquisa de bacilos álcool-ácido resistentes (BAAR), com sensibilidade de 75%. Indicada para todos os sintomáticos respiratórios, assim como para contatos de tuberculose pulmonar e indivíduos com alterações radiológicas. Destina-se também ao acompanhamento evolutivo dos casos, preferencialmente mensal e, obrigatoriamente, ao término do 2º, 4º e 6º mês de tratamento.
- Cultura do bacilo – Indicada quando a baciloscopia direta é persistentemente negativa, para diagnóstico de formas extrapulmonares da doença, nos casos com suspeita de resistência às drogas e nos casos de suspeita de infecção por outra espécie da micobactéria.
6.2.2 - Exame radiológico - Pode ser normal, suspeito (imagens sugestivas de processo tuberculoso ativo), com sequelas ou com imagens sugestivas de outras doenças (MS,SVS,2009)
- Alterações radiológicas mais frequentes na Tuberculose Pulmonar Primária: (CONDE, ET AL, 2009;
CAVALCANTI, 2010)
- radiografia normal em até 15% dos casos;
- opacidades parenquimatosas frequentemente unifocais, predominantemente no pulmão direito;
- opacidades arredondadas persistentes (tuberculomas), mais comuns em lobos superiores, podendo estar associadas à calcificação de linfonodos hilares;
- linfadenomegalia, na maioria das vezes unilateral. As regiões mais comprometidas são a hilar e
a paratraqueal direita. Frequentemente está associada a opacidades parenquimatosas e atelectasia
segmentar ou lobar.
- atelectasia decorrente da compressão extrínseca das vias aéreas por linfadenomegalias.
- padrão miliar, com pequenas opacidades nodulares, na maioria da vezes distribuídas de forma simétrica, podendo ser acompanhadas por linfadenomegalias.
- derrame pleural, manifestação tardia da tuberculose primária, ocorre em 25% dos casos.
- Alterações radiológicas mais frequentes na Tuberculose Pulmonar Pós-primária: (CONDE, ET AL, 2009;
CAVALCANTI, 2010)
- alterações parenquimatosas nodulares agrupadas, de limites imprecisos, nos ápices pulmonares e regiões infraclaviculares e intercleido-hilares;
- linhas e faixas de permeio a opacidades parenquimatosas;
- cavidade, única ou múltipla, localizada preferencialmente em segmentos apicais e dorsais, é o padrão clássico da tuberculose pós-primária. Raramente tem nível líquido em seu interior;
- após a cura, as lesões tornam-se fibróticas, eventualmente calcificadas, associadas com distorção da arquitetura parenquimatosa, bronquiectasias de tração, desvio das estruturas
mediastinais e tuberculomas;
5
- apresentações atípicas se localizam em segmentos anteriores dos lobos superiores e em segmentos basais, sobretudo em imunossuprimidos;
- presença de atelectasias.
6.2.3 - Tomografia computadorizada de Aparelho Respiratório (CONDE, ET AL, 2009; CAVALCANTI, 2010)
Indicada em sintomáticos respiratórios com baciloscopia negativa no escarro ou incapazes de fornecer material para exames micobacteriológicos, quando a radiografia é insuficiente para o diagnóstico. No atual contexto epidemiológico, o aspecto de árvore em brotamento é fortemente indicativo de tuberculose pulmonar.
6.2.4 - PPD (Derivado Proteico Purificado) (MS, SAS,DAB, 2008, Bacha, 2005, MS,SVS,2009, CONDE, et al, 2009; CAVALCANTI, 2010)
Indicado como método auxiliar no diagnóstico da tuberculose, sobretudo em pessoas não vacinadas com BCG-Id ou indivíduos infectados pelo HIV. Isoladamente, quando positivo, indica apenas a presença de infecção, ou seja, tuberculose latente, não sendo suficiente para o diagnóstico da tuberculose doença.
O resultado é expresso em milímetros de endurecimento, não sendo mais utilizada a classificação forte ou fraco reator. A tendência cada vez maior tem sido valorizar o ponto de corte de 5 mm no PPD, para diagnóstico de tuberculose latente, conforme se segue:
- 0 a 4 mm - indivíduo não infectado pelo M. tuberculosis ou com hipersensibilidade reduzida;
- > 5 mm - indivíduo infectado pelo M. tuberculosis (doente ou não), ou indivíduo infectado por outras micobactérias, ou ainda indivíduo vacinado com BCG-Id nos últimos dois anos.
6.2.5 - Outros recursos diagnósticos
Na suspeita de tuberculose extrapulmonar e tuberculose pulmonar não diagnosticada pelos métodos anteriores, outras técnicas podem ser utilizadas:
- broncoscopia com lavado e/ou biópsia, colonoscopia com biópsia; trânsito de delgado;
- exame liquórico ou de líquidos pleural, peritoneal, pericárdico e sinovial;
- ultrassonografia, tomografia computadorizada, ressonância nuclear magnética;
- exames citológicos e histopatológicos
- amplificação de ácidos nucléicos (AAN) ou reação de polimerase em cadeia (PCR);
- adenosina deaminase (ADA)(Morisson & Neves,2008) ;
- determinação do interferon gama.
7. Tratamento da tuberculose doença ( MS, SVS, DVE, PNCT, 2009, MS,SVS,2009, CONDE et al, 2009, CAVALCANTI, 2010)
Apesar de potencialmente grave, a tuberculose é passível de cura através de tratamento quimioterápico ambulatorial, que permite anular em poucos dias ou semanas(MS,SVS,2009) as fontes de infecção, representadas pelos indivíduos bacilíferos. A hospitalização é excepcional, estando restrita às seguintes situações:
- meningite tuberculosa;
- indicação cirúrgica;
- intolerância medicamentosa incontrolável ambulatorialmente;
- intercorrências clínicas ou cirúrgicas graves;
- estado geral que não permita tratamento ambulatorial;
- casos de exclusão social, como ausência de residência fixa;
- grupos com maior possibilidade de abandono, especialmente em retratamento ou falência.
Em 2009, o Programa Nacional de Controle da Tuberculose (PNCT) do Ministério da Saúde alterou o protocolo de tratamento de indivíduos com 10 anos ou mais, com previsão de introdução de novo esquema básico, já utilizado mundialmente. Ocorrerão mudanças também no retratamento de casos e no tratamento da tuberculose resistente. Tal protocolo encontra-se em vias de implantação, na dependência da capacitação dos profissionais envolvidos e disponibilização das drogas nas apresentações preconizadas.
As drogas em formulações individualizadas continuarão disponíveis para utilização em esquemas especiais.
7.1 - Esquema básico para adultos e adolescentes - Indicações:
- Casos novos * de todas as formas de tuberculose pulmonar e extrapulmonar (exceto meningoencefalite) infectados ou não pelo HIV.
* Caso novo = indivíduo que nunca usou medicamentos antituberculose ou usou por menos de 30 dias.
- Retratamento **: recidiva (independentemente do tempo decorrido do primeiro episódio) ou retorno
após abandono com doença ativa.
** Preconiza-se cultura, identificação e teste de sensibilidade em todos os casos de retratamento.

7.2 - Esquema para meningoencefalite para adultos e adolescentes (*)

7.3 - Esquema para multirresistência - Indicado nos casos de:
- resistência à rifampicina + isoniazida;
- resistência à rifampicina + isoniazida e outro(s) fármaco(s) de primeira linha,
- falência* do esquema básico ou impossibilidade do uso do esquema básico por intolerância a dois oumais fármacos.
* falência = persistência de baciloscopia positiva ao final do tratamento; baciloscopia fortemente positiva (++ ou +++) no início do tratamento, mantendo essa situação até o quarto mês de tratamento; ou positividade inicial seguida de negativação e nova positividade a partir do quarto mês de tratamento.

7.4 - Esquemas Especiais para adultos e adolescentes
Nos casos de intolerância moderada a grave, hepatotoxicidade ou hipersensibilidade, mantém-se a recomendação de reintrodução fármaco a fármaco, para a avaliação da necessidade de substituição
de algum deles.

7.5 - Reações indesejáveis ao uso dos tuberculostáticos
A maioria dos indivíduos consegue completar o tratamento recomendado, sem qualquer efeito colateral relevante. Os efeitos colaterais dos principais tuberculostáticos são classificados em menores e maiores, os quais, dependendo da intensidade, podem ser temporariamente incapacitantes.

8. Tratamento da tuberculose latente: (MS,SVS,2009; CONDE, et al, 2009)
Está indicado para indivíduos que apresentem PPD > 5 mm, história epidemiológica de contato, desde que afastada a possibilidade de tuberculose doença.
O tratamento com isoniazida, administrada em um período de 6 a 9 meses (mínimo de 180 doses), reduz em 60 a 90% o risco de adoecimento.
Pelo elevado risco de hepatotoxicidade, a indicação do tratamento leva em conta a idade do indivíduo, a probabilidade de infecção latente e o risco de adoecimento. Esse risco está na dependência da presença de comorbidades e/ou outras situações, classificadas como:
- Alto risco : HIV / AIDS; transplantados em terapia imunossupressora; silicose; insuficiência renal em diálise; neoplasia de cabeça e pescoço; contatos de bacilíferos; infecção latente adquirida recentemente (há menos de 2 anos); alterações radiológicas fibróticas sugestivas de sequela de TB;
uso de inibidores do TNF-α1; indígenas.
- Risco moderado : uso de corticosteróides (>15mg de prednisona por >1 mês); diabetes mellitus; crianças que adquiriram infecção latente até os 4 anos.
- Risco leve : baixo peso (
- Risco muito baixo : Indivíduo com infecção latente, sem fatores de risco e com Rx de tórax normal.
Assim, são elegíveis para receber o tratamento da tuberculose latente:
- indivíduos com mais de 65 anos e alto risco de adoecimento;
- indivíduos entre 50 e 65 anos e risco de adoecimento moderado ou alto;
- indivíduos com menos de 50 anos e risco de adoecimento leve, moderado ou alto.
Parte II - Considerações Médico-Periciais na Tuberculose
A incapacidade laborativa na tuberculose, para fins de estabelecimento ou prorrogação de prazos de afastamento, está na dependência da eliminação de bacilos, com potencial risco para terceiros, localização e gravidade da doença, intolerância aos tuberculostáticos, estado geral do indivíduo e exigências físicas para a atividade exercida.
Neste sentido, a forma pulmonar bacilífera é incapacitante nas fases iniciais, por curto prazo, mesmo que a tosse produtiva seja a única manifestação, sem outros comprometimentos debilitantes.
Para as formas pulmonares não bacilíferas e extrapulmonares, a intensidade das manifestações clínicas, quando relevante, determinará a incapacidade laborativa, também em geral por curto prazo.
Quando o requerente fizer jus a benefícios previdenciários ou assistenciais, uma das condições para a concessão e manutenção, atendidos os demais critérios clínicos e legais, deve ser o cadastro e acompanhamento regular no Programa de Controle de Tuberculose e/ou serviços por ele referenciados, passíveis de serem confirmados através da SIMA (Solicitação de Informações ao Médico Assistente). Esses serviços de referência estão habilitados a informar sobre os casos, recidivas e resistências, em tratamento.
Destaque-se que o controle da negativação do exame bacteriológico é responsabilidade da área assistencial.
A persistência da positividade deve estar comprovada, mediante relatório detalhado da Programa de
Controle de Tuberculose e/ou serviços por ele referenciados, não sendo suficiente a simples apresentação da baciloscopia positiva para fins de prorrogação de prazos do benefício.
O mesmo entendimento é válido para os efeitos adversos surgidos no decorrer do tratamento




Referências
BACHA, HA. Tuberculose: Diagnóstico e Tratamento. Prática Hospitalar, Ano VII, n.42, Nov-Dez,2005.
BRASIL. Decreto nº 3.048, de 6 de maio de 1999. Aprova o Regulamento da Previdência Social e dá outras
providências. Brasília: DOU 7 Mai 1999, republicado no DOU de 12 Mai 1999, retificado nos DOU 18 e 21 Jun
1999. Disponível em http://www4.planalto.gov.br/legislacao/legislacao. Acessado em Ago 2008.
______Decreto nº 6.214, de 26 de setembro de 2007. Regulamenta o benefício de prestação continuada da
assistência social devido à pessoa com deficiência e ao idoso de que trata a Lei nº 8.742, de 7 de
dezembro de 1993, e a Lei no 10.741, de 1o de outubro de 2003, que acresce parágrafo ao art. 162 do
Decreto no 3.048, de 6 de maio de 1999, e dá outras providências. Brasília: DOU 27 Set 2007.
Disponível em http://www.presidencia.gov.br/legislacao. Acessado em Ago 2008.
______Decreto nº 6.564, de 12 de setembro de 2008. Altera o Regulamento do Benefício de Prestação Continuada, aprovado pelo Decreto no 6.214, de 26 de setembro de 2007, e dá outras providências.
Brasília: DOU 15 Set 2008. Disponível em http://www.presidencia.gov.br/legislacao. Acessado em Jan 2009.
______Lei nº 7.713, de 22 de dezembro e 1988. Altera a legislação do imposto de renda e dá outras providências.
Brasília: DOU 23 Dez 1988. Disponível em http://www.presidencia.gov.br/ legislacao. Acessado em Jul 2009.
______Lei nº 8.213, de 24 de julho de 1991. Dispõe sobre os Planos de Benefícios da Previdência Social e dá outras providências. Brasília: DOU 25 Jul 1991, republicada DOU 11 Abr 1996 e DOU 14 Ago 1998. Disponível em http://www.presidencia.gov.br/legislacao. Acessada Ago 2010.
______Lei nº 8.742 de 07 de dezembro de 1993. Dispõe sobre a organização da Assistência Social e dá outras providências. Brasília: DOU 7 Dez 1993. Disponível em http://www.presidencia.gov.br/legislacao.
Acessado em Ago 2008.
______Lei nº 12.435 de 06 de julho de 2011. Altera a Lei nº 8.742, de 7 de dezembro de 1993, que dispõe sobre a organização da Assistência Social. Brasília: DOU 7 Jul 2011. Disponível em http://www.presidencia.gov.br/legislacao. Acessado em Jul 2011.
BRASIL, MINISTÉRIO DA SAÚDE, FUNDAÇÃO NACIONAL DE SAÚDE, CENTRO NACIONAL DE EPIDEMIOLOGIA.
Tuberculose – Guia de Vigiância Epidemiológica. São Paulo: J. bras. Pneumol. Jun 2004; 204(30) suppl.1.
Disponível em http://www.scielo.br/scielo.php?pid=S1806-37132004000700003&script=sci_arttext. Acessado em 03 Dez 2009.
BRASIL, MINISTÉRIO DA SAÚDE, SECRETARIA DE ATENÇÃO À SAÚDE, DEPARTAMENTO DE ATENÇÃO BÁSICA.
Vigilância em Saúde: Dengue, Esquistossomose, Hanseníase, Malária, Tracoma e Tuberculose. Brasília
13
: MS, SAS, DAB, 2008 - 2. ed. rev. 195 p. : il. (Série A. Normas e Manuais Técnicos) (Cadernos de Atenção Básica, n. 21)
BRASIL, MINISTÉRIO DA SAÚDE, SECRETARIA DE VIGILÂNCIA EM SAÚDE, DEPARTAMENTO DE VIGILÂNCIA EPIDEMIOLÓGICA. Situação da Tuberculose no Brasil. Brasília: DEVEP/SVS/MS, sd. (26 slides).
Disponível em: http://portal.saude.gov.br/portal/arquivos/pdf/apresentacao_ tb_2009.pdf. Acessado em 10 Jun 2009.
BRASIL, MINISTÉRIO DA SAÚDE, SECRETARIA DE VIGILÂNCIA EM SAÚDE, DEPARTAMENTO DE VIGILÂNCIA
EPIDEMIOLÓGICA, PROGRAMA NACIONAL DE CONTROLE DA TUBERCULOSE. Nota Técnica sobre as mudanças no tratamento da tuberculose no Brasil para adultos e adolescentes. Brasília: MS, SVS, DVE, PNCT, 2009. Disponível em: http://portal.saude.gov.br/portal/arquivos/pdf/nota_tecnica_versao _28_de_agosto_v_5.pdf. Acessado em 31 Ago 2009.
BRASIL, MINISTÉRIO DA SAÚDE, SECRETARIA DE VIGILÂNCIA EM SAÚDE. Tuberculose. In: Guia de Vigilância Epidemiológica. Brasília: Ministério da Saúde, Secretaria de Vigilância em Saúde, 2009. Disponível em: http://portal.saude.gov.br/portal/arquivos/pdf/gve_7ed_web_atual_tuberculose.pdf (acessado em 12 Jan 2010).
BRASIL, MINISTÉRIO DO DESENVOLVIMENTO SOCIAL E COMBATE À FOME; INSTITUTO NACIONAL DO SEGURO SOCIAL. Portaria Conjunta MDS/INSS nº 1, de 24 de maio de 2011. Estabelece os critérios, procedimentos e instrumentos para a avaliação social e médico-pericial da deficiência e do grau de incapacidade das pessoas com deficiência requerentes do Benefício de Prestação Continuada da Assistência Social, revoga com ressalva a Portaria Conjunta MDS/INSS nº 01, de 29 de maio de 2009, e dá outras providências. Brasília: DOU, 26 Mai 2011. Disponível em http://www.mds.gov.br/sobreoministerio/legislacao/assistenciasocial/portarias/2011. Acessado em Jul 2011.
BURGESS LJ, SWANEPOEL CG, TALJAARD JJ. The use of adenosine deaminase as a diagnostic tool for peritoneal tuberculosis. Tuberculosis (Edinb). 2001;81(3):243-8.
CABRAL, M.M.L. et al. Espondilite tuberculosa em adolescente. J Bras Pneumol 2005; 31(3): 261-4.
CAVALCANTI, E.F.A. Destaques da III Diretrizes para Tuberculose. MedicinaNet, 11 Jan 2010. Disponível em: http://www.medicinanet.com.br/conteudos/artigos/2695/destaques_da_iii_diretrizes _para_tuberculose.htm.
Acessado em: 13 Jan 2010.
CONDE, M.Barreto et al. III Diretrizes para Tuberculose da Sociedade Brasileira de Pneumologia e Tisiologia.
J Bras Pneumol. 2009;35(10):1018-1048.
FAUCI, A.S. et al. Tuberculosis. In: Harrison's Principles of Internal Medicine, 17e, section 8; chapter 158.
Disponível em http://www.msdonline.com.br/profissionais_de_saude_anon/biblioteca_anon/paginas/harrisons_online.aspx. Acessado em Jan/2010.
MORISSON, P. & NEVES, D.D. Avaliação da adenosina desaminase no diagnóstico da tuberculose pleural:
uma metanálise brasileira. São Paulo: J. bras. pneumol. [online]. 2008, vol.34, n.4, pp. 217-224. ISSN 1806-3713.
NUNES, C. et al. Fatores prognósticos de letalidade na meningoencefalite tuberculosa. São Paulo: Arq. Neuro-Psiquiatr. 56(4), Dez 1998a.
NUNES, C.et al. Meningoencefalite tuberculosa: avaliação de 231 casos. Rev Soc Bras Med Tropical. 31(5):441-447, set-out, 1998b.
PAES, A.L.V. et al. Tuberculose Ganglionar Periférica – Aspectos clínico-epidemiológicos. Belém: Revista Paraense de Medicina, vol. 20, n.4, pp 33-37, Jul-Set 2006.
UNAIDS. Frequently asked questions about tuberculosis and HIV. Disponível em
http://data.unaids.org/pub/factsheet/2006/tb_hiv_qa.pdf Acessado em 12 Jun 2009.